動脈硬化が話題になる時、ほとんどの場合、注目されるのは「悪玉コレステロール」です。
しかし、よく調べてみると、「コレステロール元凶説」はどれも信憑性に欠けていました。
絶対に悪い結果になるような不自然な条件で実験を行なったり、都合のいいデータだけを根拠に論文をまとめたり・・・と、真面目に真実を追究する姿勢ではありませんでした。
そういう歴史があるので、私は「コレステロールを悪く言う」説に対しては常に疑いを持っています。どんな新説であろうとです。
そもそも、動脈硬化は血管の疾患なので、血管そのものにもっと目を向けるべきではないでしょうか。
なので、本記事では、「動脈硬化の原因に、本当にコレステロールが関係しているのかどうか」と、「血管はどうやって劣化していくのか」に焦点を当ててお話します。
スポンサーリンク
動脈硬化について
本題に入る前に、動脈硬化がどういうものなのか、簡単に説明しておきます。
動脈硬化には3タイプあります。
- アテローム性動脈硬化(粥状動脈硬化)
- 細動脈硬化
- 中膜石灰化硬化(メンケベルグ硬化)
一般的に言う「動脈硬化」とは、「アテローム性動脈硬化」の事を指している場合が多いです。「脳梗塞」や「心筋梗塞」の原因になります。
なので、ここからは「アテローム性動脈硬化」に焦点を当てます。
アテローム性動脈硬化とは
「アテローム性動脈硬化」は、一言で言うと、血管の中に「お粥状の塊」ができた状態です。
その塊の事を、「アテローム性のプラーク(粥状の隆起)」とか、「粥腫(じゅくしゅ)」と呼びます。
アテローム性動脈硬化
アテローム性動脈硬化とは、動脈の内側に粥状(アテローム性)の隆起(プラーク)が発生する状態。
「お粥状」・・・といっても、内訳は脂質やカルシウム等です。
病理学においてアテロームとは、脂質(コレステロールや中性脂肪)、カルシウムや様々な線維性結合組織を含んだ細胞(ほとんどマクロファージ)や細胞の死骸から構成された動脈血管内での蓄積物であり固まりである。
心臓や動脈で問題になるアテロームは、通常、粥腫である。
アテロームは、不健康な状態であるが、ほとんどの人で見つかっている。
アテローム性動脈硬化の成り立ち
意味を理解したところで、次は「アテローム性動脈硬化」がどのようにしてできるのか説明していきます。
以下は、動脈の大まかな構造になります。血管の壁に注目して下さい。
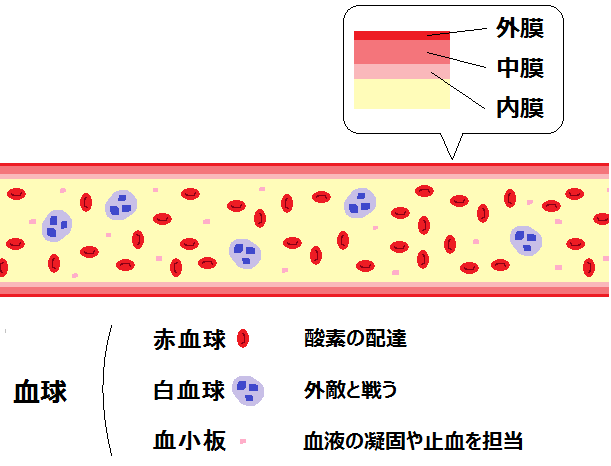
動脈硬化に関係があるのは、「内膜」と「中膜の内半分」です。膜はさらに複雑になっていますが、後で詳しく説明しますので、ここではシンプルに考えて下さい。
そして、以下が一般的に言われている「アテローム性動脈硬化」の成り立ちになります(※つまり、「アテローム性のプラーク」の出来方です)。
①「血管」は血圧が高かったり、喫煙することで内膜の「内皮細胞」が傷つけられる
↓
②傷ついた「内皮細胞」の隙間から、LDL(悪玉)コレステロールが内膜の内側に入り込んでいく
↓
③内皮細胞の内側に入り込んだLDLは、活性酸素によって酸化される
↓
④不要な酸化LDLを排除する為に、単球(白血球の一種)も内膜の内側へ入っていく
↓
⑤「内皮細胞」の間から内膜へと入り込んだ単球は、「マクロファージ」の姿に変身して掃除を行なう
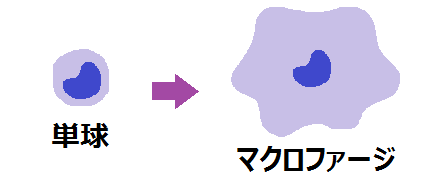
↓
⑥マクロファージは、次々と酸化LDLを食べていくので大きくなる(泡沫細胞という)
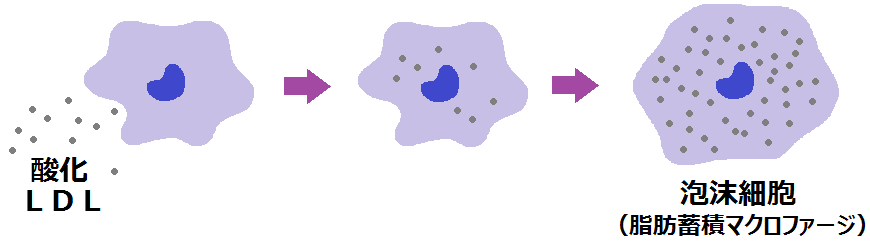
↓
⑦泡沫細胞が蓄積すると、アテロームになる
↓
⑧アテロームができると、血管壁が厚くなって、血管内部は狭くなる
あなたは、この過程を読んでどう思われましたか?
私は①の「内膜の傷が悪い」と思うのですが、
②以降の「LDL(悪玉)コレステロールが悪い」と考える人も多いのではないでしょうか。「コレステロール元凶説」は根強いですからね。
なので、先に「LDLコレステロール」について話をします。
スポンサーリンク
コレステロールとは
テレビ等で「LDLコレステロール」が紹介される時、その絵は悪者のように描かれています。あのせいで、「LDLコレステロール」に対しておかしな先入観を持っている人は少なくないと思います。
なので、コレステロールがどういうものなのかを説明します。
コレステロールは、血液の中に単体で存在しているのではありません。コレステロールは、中性脂肪やタンパク質(アポタンパクと言う)とセットになって存在しています。
このセットを「リポタンパク」と呼びます。
このような姿で血液の中に存在しているのは理由があります。
血液は水分で、コレステロールは脂です。水と脂は馴染みません。
だから、水と馴染みにくい「エステル型コレステロール」と「中性脂肪」は、比較的水と馴染みやすい「遊離型コレステロール」「リン脂質」「アポたんぱく」にくるまれることによって、血液の中に存在しているというわけです。
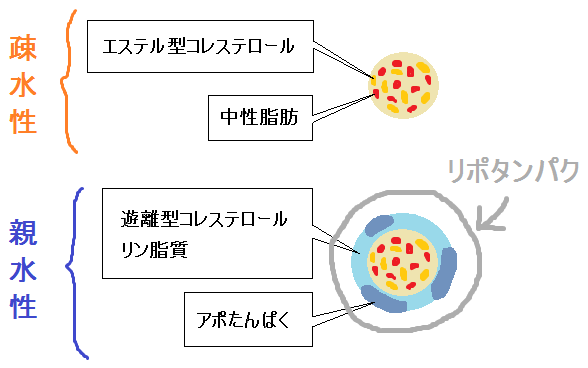
日常的に使われている「善玉コレステロール」とか、「悪玉コレステロール」といった言葉は、この加工された「リポタンパク」のことを指していて、「コレステロール分子」自体を指しているわけではありません。
リポタンパクの種類
このリポタンパク(一般的に言うコレステロール)は、善玉と悪玉の他にもいくつかあります。
- (カイロミクロン(キロミクロン)/ 英語:chylomicron)
- (超低比重リポタンパク / 英語:Very-Low-Density Lipoprotein cholesterol)
- (中間比重リポタンパク / 英語:Iintermediate Density Lipoprotein cholesterol)
- (低比重・リポタンパク /英語:Low-Density Lipoprotein cholesterol)→ 悪玉コレステロール
- (高比重リポタンパク / 英語:High Density Lipoprotein cholesterol)→ 善玉コレステロール
脂質の比率や密度、合成される場所によって、このように分けられています。
様々なサイトを参考に、それぞれのサイズを図にしておきました。一番小さいのが善玉と呼ばれる「HDLコレステロール」です。
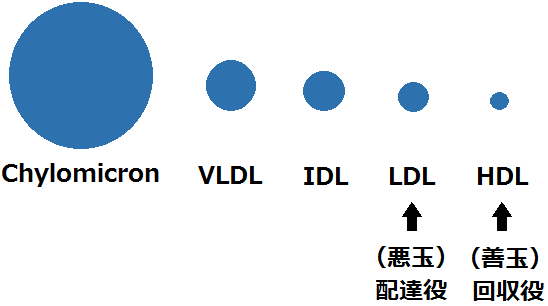
で、本題は悪玉と呼ばれる「LDLコレステロール」・・・でしたね。
なので、次は先ほど書いた、アテローム性動脈硬化の成り立ちの↓この部分を詳しくみていきます。
②傷ついた「内皮細胞」の隙間から、LDL(悪玉)コレステロールが内膜の内側に入り込んでいく
有益なLDLコレステロールが悪いと言われる理由
ここからはリポタンパクの中で2番目に小さい「LDLコレステロール(ロウ・デンシティ・リポプロテイン・コレステロール)」が本当に悪いのか検証していきます。
LDLコレステロールは「悪玉」などと呼ばれていますが、「新鮮なコレステロールを全身に配達する」という体にとって重要な役割を担っています。
良い仕事をしているのです。
よくよく調べてみると、「LDLコレステロール」そのものが悪いのではなく、「変性したLDLコレステロール」が悪いのだそうです。
〇 正常なLDLコレステロール
× 変性したLDLコレステロール
そして、「変性したコレステロール」にもいくつかパターンがあるみたいですが、多くは活性酸素によって酸化したLDLコレステロールだそうです。
「正常なLDLコレステロール」は、マクロファージに相手にされませんので、先ほどお話した「泡沫細胞」を作ることはありません。
しかし、「酸化したLDLコレステロール」は毒性が強く、マクロファージから見ると有害物質なので、食べられます。すると、「泡沫細胞」を作って動脈硬化を進行させてしまいます。
「酸化LDLコレステロール」が危険視されているのは、以上の理由からです。
では、何故、LDLコレステロールは酸化してしまうのか・・・その理由が気になると思うので解説します。
スポンサーリンク
LDLコレステロールが酸化する理由
実は、「悪玉」と呼ばれるLDLコレステロールは、2種類あるそうです。
- 通常サイズの LDLコレステロール
- 小型サイズの LDLコレステロール(small dense LDL スモール・デンス・LDL)
後者を、超悪玉コレステロールと呼びます。
そして「小型LDLコレステロール」が「超悪玉」と言われる根拠が以下になります。
『川村内科診療所 脂質代謝系 2015年5月19日 火曜日 小型LDLの重要性 平野勉教授』より引用
① 血液中に滞在する時間が、通常のLDLの場合は平均2日なのに比べ、5日と長いこと
② 血管壁のプロテオグリカンに付着しやすいこと
③ 小型の粒子なので血管内皮下に侵入しやすいこと
④ 通常のLDL粒子に比較してコレステロール含有量が少ないが、それ以外にも脂溶性の抗酸化ビタミンなどの抗酸化物質が乏しいため酸化されやすい
⑤ 酸化されるとマクロファージに取り込まれ、泡沫化し、動脈硬化層へと進展していく
『生研 small, dense LDL はなぜ動脈硬化惹起性が強いのでしょうか?』より引用
small, dense LDL(sd LDL)は、LDL を異化する LDL レセプターに対する親和性が低下しており、血中滞在時間の長いことが知られています。
一般的に正常サイズの LDL の血中滞在時間は2日、sd LDL のそれは5日と言われています。このため、sd LDLは血管壁と接触する機会が多いと言えますが、それ自身が小型であることと相まって血管壁に侵入しやすく、酸化変性というストレスにさらされやすいという側面を有しています。
さらにこの酸化ストレスに対して、正常サイズの LDL はビタミン E やユビキノール10といった抗酸化物質によって保護されていますが、sd LDL は抗酸化物質に乏しく酸化変性を受けやすいという特徴も有しています。
以上のことから、sd LDLはアテローム性動脈硬化の主因である酸化LDLの良き原料と考えられています。
「小型LDLコレステロールの特徴」と、それによる不都合な展開を完結にまとめるとこうなります。
- 滞在時間が長い → 血管壁と接触する機会が多い
- サイズが小さい → 血管壁に侵入しやすく、侵入した先で酸化される
- 抗酸化物質が乏しい → 活性酸素に対する防御力が弱いので酸化しやすい
「小型LDLコレステロール」は、このような条件がそろっているので、毒性の強い「酸化コレステロール」になりやすいというわけです。だから「超悪玉」と言われています。
「小型LDLコレステロール」は、よく「小型だから悪い」と言われていますが、厳密に言うと「内皮細胞に入ると酸化するから悪い」ということになります。
以上が「LDLコレステロールは動脈硬化の原因になる」・・・と悪く言われる所以です。
しかし、忘れてはいけません。
酸化コレステロールは泡沫細胞の蓄積を招くので「アテローム性動脈硬化」を進展させますが、あくまで二次的なものです。
コレステロールの前に注目しなければいけない過程があります。
それが、最初に起こる「内膜の傷」です。
内膜の傷
確かに、酸化コレステロールは良くない性質をもっています。
しかし、元になった「小型LDLコレステロール」を溜めない事が動脈硬化を防ぐ一番の方法か・・・というと、私はそうは思いません。
コレステロールに気をつけるよりも、①の血管そのものの健康に気をつける方が、根本的な解決に繋がると思うのです。
その根拠をお話します。ここでもう一度、「アテローム性動脈硬化」の流れを見て下さい。
①「血管」は血圧が高かったり、喫煙することで内膜の「内皮細胞」が傷つけられる
↓
②傷ついた「内皮細胞」の隙間から、LDL(悪玉)コレステロールが内膜の内側に入り込んでいく
↓
③内皮細胞の内側に入り込んだLDLは、活性酸素によって酸化される
↓
・・・
そもそも、①が起こらなければ「内皮細胞」は傷つかないということになりますよね。
そして、「内皮細胞」が傷つかなければ、「小型LDLコレステロール」が隙間から入ることもありません。
そして、LDLコレステロールの酸化は「内皮細胞」に入り込んだ先で起きるので、入り込まなければ酸化LDLコレステロールは作られない・・・ということになります。
マクロファージは「酸化LDLコレステロール」にならなければ攻撃してこないそうなので、その後の「泡沫細胞」になる展開も起こりません。
結局、元をたどれば「血管にLDLが入ってしまう傷ができる事」、「内皮細胞に入ってしまう事」が悪いのであって、「小型LDLコレステロールが悪い」・・・というのはなんか違うような気がします。コレステロールに関する説はインチキが多いので、無駄に大騒ぎしすぎかなと思います。
しかし、既に内皮細胞に傷が多い人は、小型LDLが入り込む確率が増しますし、そうなれば酸化してマクロファージの攻撃対象ですから、どうにもなりません。その場合は小型LDLコレステロールを減らす努力をした方が良いでしょう。
また、「小型だから内皮細胞に入りやすい」・・・ということですが、それを言うなら「HDL(善玉)コレステロール」も小型です。何故こちらは内皮細胞に入っていかないのか・・・
謎はありますが、とりあえずコレステロールの話は置いておいて、ここからは「血管の状態」に注目します。
血管の状態に注目する
「動脈硬化」という疾患は「血管の症状」なので、そこを流れている「コレステロール」に注目するよりも、「血管の質」そのものに目を付ける方が理に適った分析だと思います。
動脈硬化を予防したい人は、コレステロールの心配をする前に、血管の質が悪くならないような生活を心がけた方が良いでしょう。
しかし、その為には、何故、血管の質が悪くなるのかについて知っておく必要があります。
まずは、コレステロールから頭を切り替える為に以下をお読み下さい。
『日本人よコレステロールを恐れるな / 著者:長谷川元治』より引用
「コレステロールが高い=動脈硬化」ではない。
みなさんが健康診断などを受けたとき、コレステロールが高いと、動脈硬化を起こしている(あるいは起こすおそれがある)と言われます。しかし、実はここに大きな落とし穴があるのです。
たとえば、高血圧かどうかを調べるときには血圧そのものを測定します。その結果、血圧の値が高かった人がすなわち高血圧ということになります。血圧が高いことを高血圧というのですから、これはあたりまえです。
ところが、動脈硬化の場合は違います。血管の病変であるにもかかわらず、血管そのものをなんらかの形で検査。測定するのではなく、血中コレステロールという“別のもの”を測って、間接的に診断を下しているにすぎません。
これば、血管そのものの状態を直接調べる簡易な検査法が少なく、行なう場合には特別な機器や技術が必要だったため、会社や地域の健康診断や人間ドックなどで実施しにくかったという事情もあるでしょう。
しかし、その結果、不幸なことに「コレステロールが高い=動脈硬化」という図式が世の中に浸透してしまいました。
本来、血中コレステロールが高いということは、血液中にコレステロールが多いという状態を示しているにすぎず、それ以上でも以下でもありません。
血管の状態そのものは調べていないのですから、動脈硬化かどうかはほんとうにはわからないはずです。にもかかわらず、わかったことにしている、つまり動脈硬化を起こしている(起こすおそれがある)とみなしているのが現在行なわれている検査・診断であるといえるでしょう。
実際には、コレステロールが高くても動脈硬化を起こさない例があり、逆にコレステロールが低くても動脈硬化を起こしている例も多いことがさまざまな研究・調査によって、また私自身の研究によっても明らかになっています。
(p37~38p)
こちらは、1998年に出版された本です。言うまでもありませんが、あの当時「動脈硬化はコレステロールが原因ではない」という説を唱えるのは凄いことです。
ですが、ここに書かれてある内容は、考えたら当たり前のことです。小学生でも分かる理屈ではないでしょうか。
しかし、みんなが「動脈硬化=コレステロール」と言うと、なんとなく「そうかな・・・」と思うようになるのです。
スポンサーリンク
動脈硬化の定義
動脈硬化が何かよく分かっていないと原因もわかりません。
なので、まず動脈硬化の定義をハッキリさせます。
血管の“しなやかに伸び、力強く復元する”という機能が失われる。
動脈硬化とは何かという問題を考えるとき、二つの側面からのアプローチがあります。
一つは“血管機能”の面から論じる場合、もう一つは“病理組織学”の面から検討した場合です。
このうち、血管機能の面から動脈硬化を論じるのは、実はそれほどむずかしいことではありません。一言で言えば、動脈が本体持っている「しなやかに伸び、力強く復元する」という機能が低下し、失われた状態を動脈硬化と呼ぶのです。
(中略)
正常な動脈、よい動脈とは何でしょうか。
医学的にいろいろな側面から表現することはできますが、要はこの“しなやかに伸び、力強く復元する”機能を維持しているということに尽きるでしょう。
動脈硬化を起こすと、血管はこのような機能を失ってしまいます。
実際、不幸にも亡くなられたかたがたの大動脈をとり出し、手で引っぱってみると、正常な血管は柔らかくて、よく伸びるのですが、動脈硬化を起こした血管はガチガチに硬く、まったく伸びません。
こうした状態では、動脈は血液を全身のすみずみまでつつがなく送り届けるという大事な役目を果たすことができなくなってしまいます。
(139p~142p)
機能的に良い動脈がどういう状態か分かったので、次は顕微鏡を使って病気の細胞と組織を検査する「病理組織学」から見た動脈硬化の定義をみていきます。
冒頭でも少し解説しましたが、動脈壁は、「内膜」、「中膜」、「外膜」の3つに分けられます。
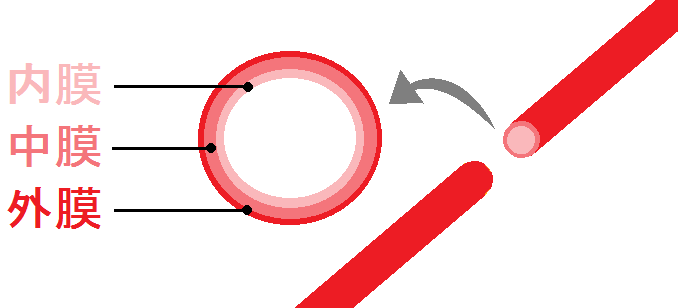
この構造を頭に入れた上で続きをお読み下さい。
動脈硬化とは血管の組織が“病的老化”を起こした状態。
一方、病理組織学の面から見た場合はどうでしょうか。こちらは実はなかなかむずかしい問題なのですが、できるだけわかりやすく説明してみたいと思います。
動脈の血管壁の組織は、内膜、中膜、外膜という三つの層を重ね合わせた形でできています。
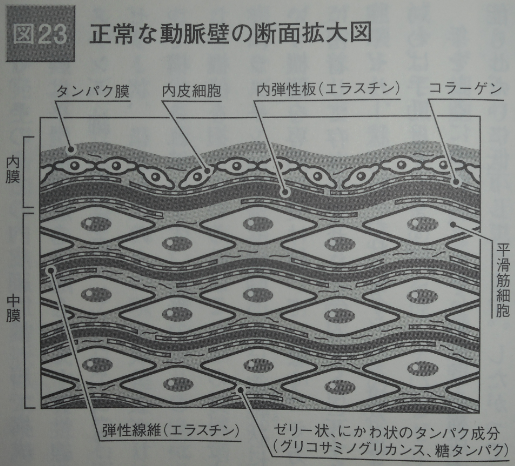
このうち、動脈硬化に関係が深いのは内膜と中膜(の内側半分)です。図23に正常な動脈の断面拡大図を示しました。
内膜は表面のタンパク膜、内皮細胞、内弾性板(エラスチン)から成り立っており、そのうちの内皮細胞は一層で構成されています。
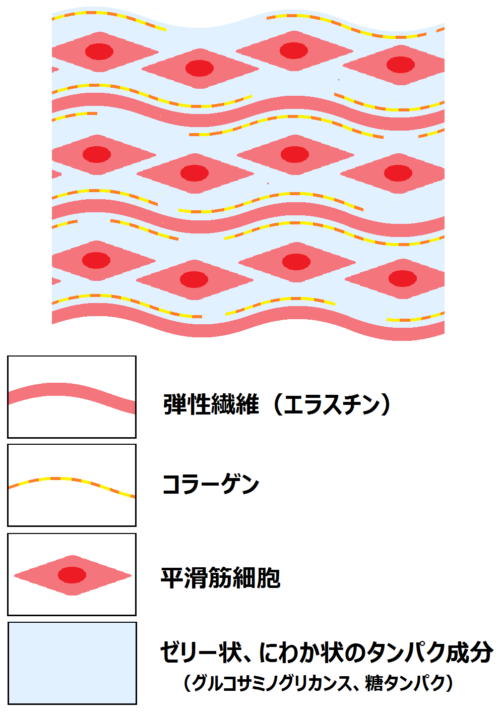
中膜は平滑筋細胞を中心として、弾性繊維という太い線維性のタンパク質(エラスチン)、細い線維性のタンパク質(コラーゲン)、それらの間を埋めるしなやかなゼリー状、にわか状のタンパク成分(グリコサミノグリカンス、糖タンパク)によって構成されています。
動脈の「しなやかに伸び、力強く復元する」というすばらしい機能を担っているのはこれらの材料です。
エラスチンは平滑筋細胞の間に繊維状に分布しており、「しなやかに伸びる」という機能を専門に受け持っています。
一方、コラーゲンはエラスチンの要所、要所に密着して存在しており、「力強く復元する」という機能を受け持っています。細胞やゼリー状、にわか状のタンパク成分はこの二つの機能がスムーズに働くように、いわば手助けをします。
年をとるにつれて、これら動脈壁を構成する成分の形と質は徐々に劣化し、その機能もしだいに低下してきます。
したがって、結果として動脈は硬くなってきますが、そのとき“病的な成分”が発生していなければまだ「生理的老化」の段階であり、動脈硬化を起こしているとは言えません。
それに対して動脈壁に“病的な成分”が発生している場合を「病的老化」と呼び、私はこれをイコール動脈硬化と定義しています。
上の画像を参考に、「内膜」と「中膜」の構造をシンプルにしておきます。
まずは、「内膜」です。水色の部分は後で説明しますので、ここでは以下の名前を覚えて下さい。
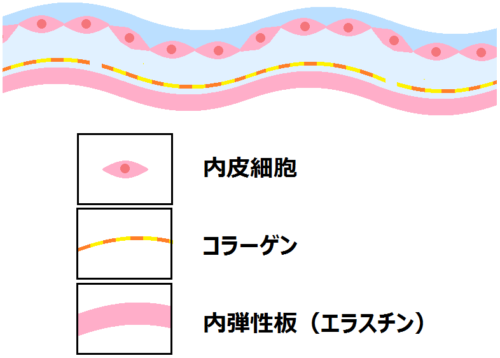
次は「内膜」です。
それぞれの役割をまとめます。
- エラスチン・・・「しなやかに伸びる」機能
- コラーゲン・・・「力強く復元する」機能
- 細胞・ゼリー状・にわか状のタンパク成分・・・2つの機能のサポート
年をとって、これらの成分、質、機能が低下したら、動脈は硬くなりますが、以下の違いがあります。
動脈壁に病的な成分が発生していない状態(動脈硬化を起こしていない)
動脈壁に病的な成分が発生している状態(動脈硬化と定義)
後者が「動脈硬化」です。
スポンサーリンク
動脈硬化のプロセス
定義がハッキリしたところで、次は動脈硬化になるプロセスです。
さっきの「アテローム性動脈硬化」のプロセスの説明では見られなかった話なので、楽しんで読んで下さい。
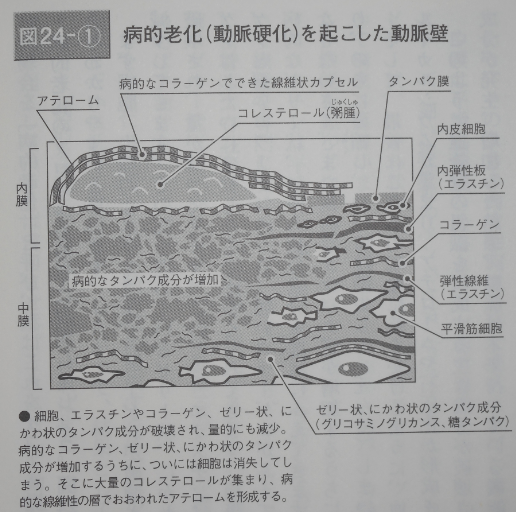
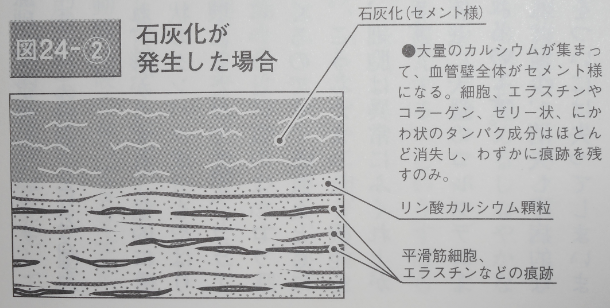
病的老化のプロセスを簡単に説明しましょう。図24―①、②をごらんになると、よりわかりやすいと思います。
まず細胞、生理的なエラスチン、コラーゲンが破壊され、形がくずれ、量的にも減少してきます。その間を埋めているゼリー状、にわか状のタンパク成分もやはり破壊され、量が減ってきます。
このとき、エラスチンは壊れるだけですが、コラーゲンはしだいに変性したものがつくられてきます。簡単にいうと、質のよいコラーゲンと悪いコラーゲンのうち、悪いコラーゲンがふえてくるのです。
それとともに病的なゼリー状、にわか状の成分も塊状にふえてきます。こうしたまったく機能をなさないさまざまな病的なタンパク質が増加するうちに、細胞は異常にふくれ上がり、のちに萎縮し、ついには消失して(死んで)しまいます。
そして、最後にこれらの現象に輪をかけるように、血管壁に大量のコレステロールやカルシウムが集まり、アテロームや石灰化が形成されるのです。
このように血管壁の組織を構成する主な成分が破壊され、減少、消失し、病的な成分が発生、増加した結果、動脈は本来持っている機能をついには失ってしまいます。
つまり、しなやかに伸びなくなり、力強く復元しなくなるのです。病理組織学の視点から論じた場合、動脈硬化はまさにこの病的老化が起きた時点をもって始まると言ってよいでしょう。
(143p~147p)
「病理組織学」の視点で見た動脈硬化のプロセスを簡単にまとめるとこうなります。
①エラスチン、コラーゲン、ゼリー状、にわか状のタンパク成分が破壊され形が崩れ、量が減少する
↓
②変性したコラーゲンが増え、病的なゼリー状、にわか状の成分は塊状に増える
↓
③病的なタンパク質の増加によって細胞が膨れ、萎縮、消失する
↓
④血管壁に大量のコレステロールやカルシウムが集まる
↓
⑤アテロームや石灰化が形成される
↓
⑥動脈は本来持っている機能を失う
どうでしょう。
先に紹介した「アテローム性動脈硬化」になるプロセスとは、ちょっと違いますね。
一般的な「アテローム性動脈硬化」の説明は、動脈壁が傷つく様子を軽く触る程度で、その後の「コレステロールが~」ばかりを強調していました。
しかし、こちらの説明では、諸悪の根源である動脈壁の変性ぶりが丁寧に描写されています。私はここがミソだと思っています。
コレステロールと関係なく動脈の変性は起こるのです。
スポンサーリンク
動脈硬化になることで失われる機能
動脈硬化になると、どんな不都合な事が起こるのかみていきましょう。
血管は「栄養呼吸」を行なっています。
しかし、病的な老化(動脈硬化)をしたものは、その機能を失ってしまうのです。以下はその実験の様子です。
私達の体を構成する組織はすべからく、栄養分や酸素をとり入れて、かわりに浪費物を排出する「栄養呼吸」を行なっています。
動脈壁のように常に動きつづけている組織の場合には、なおさらこの栄養呼吸が非常に活発に行なわれていることが予想されます。もしそうでなければ、動脈壁の組織は疲労とエネルギー不足に陥って、伸び縮みを繰り返しつづける“激務”にはとても耐えきれないはずだからです。
では、動脈壁の組織の栄養呼吸はどのような仕組みになっているのでしょうか。実は、これが動脈硬化の発生する原因を知るうえで重要なポイントになります。私たちは次のような実験を行いました。
まず人間(や動物)の動脈組織を短く切ってとり出し、それを人工心臓を中心とした特殊な装置にとりつけます。
この装置は心臓の拍動や血液を生体同様に再現する仕組みになっており、作動させると脈動流が起きて、溶液が管腔の中に送り出され、動脈の口径は体内にあるときと同様に広がったり、元に戻ったりを繰り返します。このとき、動脈の組織に必要な栄養素をとかした液体(よく見えるように着色してある)を送り出して、どうなるかを観察してみたのです。
すると、正常な動脈(や生理的老化を起こしている動脈)では、口径が広がったときに溶液が血管壁の組織に十分に吸い込まれ、元に戻るときに溶液が吐き出されることが確認できました。血管壁の断面図でいうと、中膜組織の内側半分にまで深く溶液は出入りしています。
つまり、動脈壁はその伸び縮みに連動して、実に活発に栄養呼吸を繰り返していることがわかったわけです。心臓は1日に10~11万回は拍動しますから、動脈の栄養呼吸も同じ回数だけ行なわれていることになります。
では、動脈硬化=病的老化を起こしている動脈の場合はどうだったでしょうか。同様の実験を行なってみたところ、栄養液は血管壁の組織表面の浅いところに貯留して(たまって)しまい、そこから奥には入っていきませんでした。
つまり、栄養呼吸が障害されているか、ほとんど行なえなくなっていたのです。肺呼吸になぞらえて言うと、“浅く息を吸い、浅く息を吐く”といった、まるで呼吸困難に陥った重症の肺炎のような呼吸の仕方でした。
このような状態では動脈壁の組織は栄養不足に陥ってボロボロになっていくのは当然だと言えるでしょう。
病的な老化を起こしている動脈
↓
栄養呼吸が障害される
↓
血管が栄養不足でボロボロ
・・・悪循環ですね。
ところで、もう一度言いますが、この本は1998年、今から約20年前に書かれています。
従って、所々「LDLコレステロール=悪者」という当時の概念で話を展開されていますが、「LDLコレステロールは悪くない」と事実が分かる前なので、考慮して続きを読んで下さい。
さらに、私たちは着色した「LDLコレステロール」をとかした液を使って同様の実験を行なってみました。LDLコレステロールは俗に“悪玉コレステロール”と呼ばれ、動脈壁の中に侵入してアテロームをつくる原因となり、ひいては動脈硬化を引き起こす元凶であると一般には言われているものです。
実験の結果、正常な動脈では、LDLコレステロールはまったくといってよいほど血管壁の中には侵入できませんでした。もちろん栄養呼吸は活発に行なわれているのですが、LDLコレステロールは入っていきません。
それに対して、動脈硬化を起こしている血管では、LDLコレステロールがまるで土足で人の家に踏み込むように、血管壁の組織の中に侵入していったのです。しかも、組織内に入ったLDLコレステロールはそこに居ついてしまって、外に出てくることはありませんでした。
以上の結果をまとめてみますと、正常な動脈ではスムーズに栄養呼吸が行なわれており、必要な栄養素は組織の中にとり入れられますが、LDLコレステロールは侵入できません。つまり、必要な成分は入れて、害になる成分は撃退するという一種の「取捨選択機能」(バリア)が働いているわけです。
一方、動脈硬化=病的老化を起こしている動脈では栄養呼吸はほとんど行なわれておらず、必要な栄養素を組織内にとり入れることができませんが、逆にLDLコレステロールはどんどん侵入していきます。
つまり、動脈がもともと持っているはずの取捨選択機能が壊れているわけです。
(148p~151p)
血管壁の組織の中にLDLコレステロールが入るのは良くないそうです。この点は先ほどの「アテローム性動脈硬化」の説明と同じです。
内皮細胞の中に入ると酸化されてしまいますから。
でも、ふと思いました。
「血管壁の組織の中にLDLコレステロールが入るのは良くない」・・・と言うと「入らない方がいい物質=害」と考え、「やっぱりLDLコレステロールは悪いんだ」と結論づけてしまうかもしれません。
「悪玉」という概念があると、そういう発想につながりやすいです。
しかし、「入らない方が良い」からといって、必ずしもそれが「害」だからとは限りません。
例えば、「水」は体にとって必要です。
胃の中に入れば有益ですが、肺の中に入ったら有害です。「肺に入ると悪いから、水は体に悪い」・・・ということにはなりませんよね。
それと同じように、血管壁の組織の中に「LDLコレステロール」が入らないようになっている、または、入ったら都合が悪い現象が起きるのは、
単純に、「LDLコレステロールは血管壁の組織の中に機能的に相応しくないだけ」・・・ともとれるわけです。
従って、私は小型だろうが普通サイズだろうが、以下のように捉えています。
× LDLコレステロール=有害成分
〇 LDLコレステロール=正常な血管壁の組織には不要成分
スポンサーリンク
タンパク成分の膜の存在
血液中を流れる「LDLコレステロール」が、内膜の内皮細胞の中に入ったら良くありません。
次は、血液に面している「内膜」の構造に焦点を当てます。
動脈壁の内膜の表面には「内皮細胞」がびっしり綺麗に並んでいます。
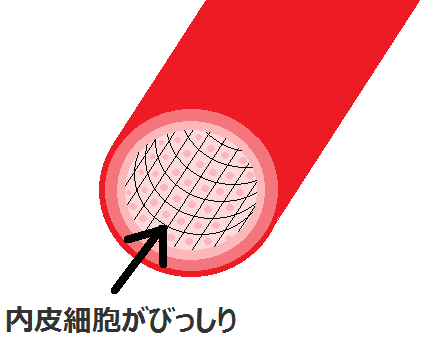
この「内皮細胞」が血液と触れている・・・と思われるかもしれませんが、そうでもないようです。
実は、「内皮細胞」の上に膜が存在しています。
血液に触れているのは「タンパク成分の膜」です。
私たちは「走査電子顕微鏡」という何千、何万倍という倍率で、しかも組織を立体的に見ることができる高性能の顕微鏡で、動物や人間の動脈をつぶさに観察しました。
その結果、動脈壁のいちばん内側、つまり血液と接している面にゼリー状、にわか状のタンパク成分(グリコサミノグリカンス、糖タンパク)でできた「膜」を発見しました。
(中略)
私たちがこの膜を発見したのは、動物実験がきっかけでした。
麻酔をしたウサギの心臓が拍動しているうちに、ごくわずかの固定液を血液中に流します。
そして、走査電子顕微鏡で動脈の組織を観察したところ、明らかに内皮細胞群の直上に膜が一面一様に存在することを確認できたのです。内皮細胞が無数に並んでいる様子を拡大してみると、まるで“キャベツ畑”のようですが、この膜はあたかも霜などの害からキャベツを守るために張られたビニールシートのようにも見えます。
その後、固定液の用い方など、実験や観察の方法にさらに工夫を重ね、他の動物や人間のいろいろな動脈の血管壁にも同様の膜が存在することを突き止めました。
(中略)
しかも、その後の研究で、タンパク膜は動脈壁の表面だけでなく、組織内のすみずみにまで張りめぐらされていることもわかりました。
先に述べた平滑筋細胞やエラスチン、コラーゲンなどの間を埋めるしなやかなゼリー状、にわか状のタンパク成分が、こうした膜の働きをつかさどっているのです。
この膜がかなり重要な役割をするのです。
しかし、「タンパク成分の膜が存在している」とハッキリと書かれている本がある一方で、「血液に触れているのは内皮細胞である」とタンパク膜がなかったかのように書かれている情報源があります。どちらかというとこちらの方が多いです。例えば、
『一生切れない、詰まらない「強い血管」をつくる本 著者:島田 和幸』より引用
内皮細胞の“バリア機能”と“活性化機能”
血管病のメカニズムを知ると、血圧や血糖値、LDLコレステロール値が高い人は、「このままでは危ないかも・・・」と不安な気分になってしまうかもしれません。
しかし、血管は、若返りが可能な器官です。
疲れて老化しかけた血管も、セルフケアで強くよみがえらせることができ、それによって怖い血管病も防げるのです!
その生まれ変わりのカギを握るのが、“内皮細胞”です。
血管壁の最も内側に位置する内皮細胞は、一層の細胞だけが並ぶ薄い層ですが、血管内腔(血管の内側の空洞)との境にあるので、血管内を流れる血液につねに接しています。
そのため、血液と血管壁の仲介者のような役割を持ち、血管を守り、強くするよう働いているのです。
バリア機能は「防壁機能」とも呼べるもので、血液中に存在する成分が血管壁内に侵入するのを防いでいます。
血液の循環を川の流れにたとえると、内皮細胞は、川の水があふれないように保ち、よどみない流れを促す堤防のようなものです。
一方、活性化機能は、内皮細胞自身が作る物質に関係しています。
内皮細胞は、防壁となって血管壁を守るだけでなく、血管を健康に保つための物質を自らが生み出し、活用しているのです。
そのおもな物質が“NO(一酸化窒素)”です。NOは排気ガスにも含まれていますが、人の体内で生み出されるNOはとても良い働きをします。
その驚くべき作用を発見した研究者はノーベル賞をもらったほどです。
内皮細胞から生まれたNOは血管壁に良い刺激を与え、血管壁を広げるよう働きます。すると、血圧が下がり、血管の負担が減ってきます。
また、NOが血液中に放出されると、血液がかたまりにくくなり、脳梗塞や心筋梗塞の引き金になる血栓(血のかたまり)ができにくくなります。
そのため、内皮細胞がイキイキしていると、血管自体も若さと強さを保てます。
逆に、内皮細胞が疲れていると、本来の役割を果たせなくなり、血管の老化が早まって、40代や50代でも血管病に襲われてしまうのです。
つまり、内皮細胞をどうケアするかが、血管ケアの最大のカギとなるのです。
違いをまとめてみます。
- 内皮細胞は血液に常に接していると書かれている
- 「バリア機能」の事には触れるが「タンパク成分の膜」は触れない
- 「活性化機能」について書かれている
気になるのは、「タンパク成分の膜」について触れられていない事です。他にもネットや本を色々探したのですが、どの情報にも書かれていません。
その後、「膜の名前が変わった」のか、「やっぱり膜はなかったことになった」のかは分かりませんが、「内皮細胞は血液に接している」というものばかりです。
長谷川氏の本には、私たちは発見したと、
「その後、固定液の用い方など、実験や観察の方法にさらに工夫を重ね、他の動物や人間のいろいろな動脈の血管壁にも同様の膜が存在することを突き止めました。」
・・・と、膜が存在していると具体的に書いてあるので、何故その他の情報に、「タンパク成分の膜」のことが記されていないのか不思議です。
しかも、「図23 正常な動脈壁の断面拡大図」には膜がハッキリと描かれています。
スッキリしませんが、先に進みます。
スポンサーリンク
タンパク膜の役割
再び長谷川氏の話に戻ります。
「タンパク成分の膜」が存在していて、どういう役割を果たしているのかをみていきます。
動脈というと堅固なゴムチューブのようなものを思い浮かべがちですが、実は拡大して見ると動脈壁の組織はスポンジのような構造になっており、無数の微小な管孔(通路)が動脈内腔(血液と接する部分)に開口しています。
栄養素などの血液成分はこの微小管孔を通って動脈壁組織の奥深くまで入っていくのですが、管孔(かんこう)の開口部も内側もすべて取捨選択機能を持ったゼリー状、にわか状のタンパク膜でおおわれており、そこでもまた、こまかな栄養呼吸が行なわれているのです。
これら動脈壁内外のタンパク膜が正常でしっかりしていれば、動脈壁の栄養呼吸はスムーズに行なわれ、必要な栄養分はとり入れられて、かわりに老廃物は排出されます。また、LDLコレステロールなどの有害な成分はシャットアウトされます。
逆に膜の質が悪くなったり、あるいは壊れたりすると動脈壁の栄養呼吸は十分に行なわれず、必要な栄養分がとり入れられなくなり、老廃物もきちんと排出できなくなります。
その結果、動脈壁の組織は栄養不足に陥ってボロボロになり、さらにはLDLコレステロールなどの有害成分も侵入してくるのです。
タンパク膜の役割です。
- 栄養呼吸(栄養を取り込み、老廃物を排出)
- 不要成分をシャットアウトするバリア機能
情報源によって、ところどころ食い違いますが、血管壁が「不要な成分をシャットアウトするバリア機能」を持っていることは確かです。
sdLDLコレステロールが酸化される場所
「バリア機能」は重要です。
100歩譲って「sd(小型)LDLコレステロール」が悪かったとしても、膜の不具合(バリア機能に問題)がなければ中に入れないので問題はないようです。
何故なら、「小型LDLコレステロール」は、血液内で酸化されるのではなく、膜に入った後で酸化されるからです。
以下の動画の0:37でも、酸化は動脈壁の内部の化学反応で起こると説明されています。その部分を文字起こししてみました。
コレステロール、脂肪、細胞はいきせい生物など、血中内を移動する物質は動脈壁の損傷領域の内部で蓄積します。
蓄積した物質内で起こる化学反応によりコレステロール分子は酸化されます。
動画がこちらです。
極端に言えば、膜がきちんと機能していて、動脈壁に入らなければ酸化されないので、血液の中に「小型LDLコレステロール」が多かろうが少なかろうが問題はありません。
少なくとも、理論上はそういう事になります。

(膜があると守られているので、LDLも単球も中には入れない)
スポンサーリンク
電気化学的な面から見た動脈硬化
余計なものが中に入らないように守ってくれている「タンパク成分の膜」ですが、どうやって不要な成分をシャットアウトしているのか、もしこれが壊れたらどうなるのかを、みていきます。
少し話がむずかしくなりますが、動脈硬化の発生・進行を電気化学的な面から説明してみましょう。
赤血球や白血球、リンパ球、血小板をはじめ、LDLコレステロールなどの有害成分も含めて、すべての血液の有形成分はマイナスの電気を帯びています。
一方、動脈壁のタンパク膜は正常な状態では電気的にはほとんどゼロ、つまりプラスもマイナスも帯びていない状態です。
したがって、血液中の成分と動脈壁のタンパク膜とは電気的にお互いに反発し合うので、くっつくことはありません。
ところが、このタンパク膜は質が悪くなったり、壊れたりすると、急速にプラスに荷電してくるのです。
そうなると、マイナス電気を帯びている血液成分とお互いに引き合うようになりますから、それらの成分がタンパク膜の表面に集まってきて、たくさんくっついてしまいます。
こうした状態がつづくと、いろいろな余計な成分が膜の上に蓄積し、さらに病的なコラーゲンなども膜の上に雑草のように生えてきて、やがて厚くて硬い層ができ上がります。
タンパク膜や内皮細胞はその下にいわば“生き埋め”になってしまうわけですから窒息状態になり、破壊され、ついには消失してしまいます。
そして、膜の消失した部分から分子量の小さいLDLコレステロールなどの有害な成分がどんどん動脈壁の中に入り込むようになるのです。
電気の状態を図にしてみました。
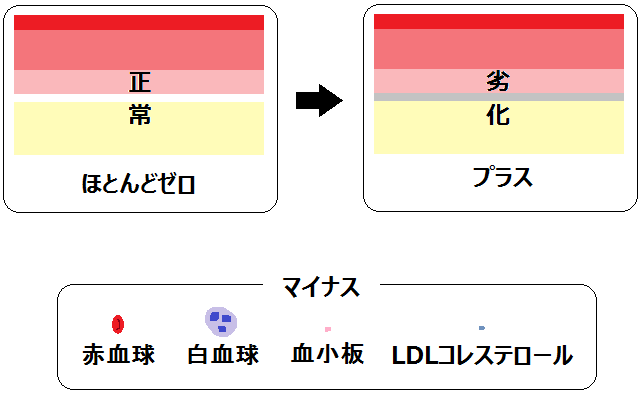
つまり、こういうことです。
①左の「正常な膜」だと血液中の成分はくっつかない
↓
②膜が劣化すると、膜と血液中の成分はくっつく
↓
③余計な成分が膜の上に蓄積する
↓
④タンパク膜や内皮細胞は、窒息、破壊、消失する
↓
⑤壊れたところから分子量の小さいLDLコレステロールが侵入
ただし、この電荷の話は分からないことが多いです。
「血液中の成分の電荷」と「動脈壁の電荷」について色々調べていたらこんな話もありました。
『CRCグループ リポ蛋白分画の検査法の違いを教えてください。』より引用
また、リポ蛋白はその表面に存在するアポ蛋白のアミノ酸残基を反映して陰性に荷電しています。
この陰性荷電はLDL、VLDL、HDLの順に増加し、CMはほとんど荷電が認められません。
「LDLコレステロール」は他のリポタンパクに比べてあまり陰性に荷電していない・・・ともとれます。
で、悪玉である「LDLコレステロール」より、善玉である「HDLコレステロール」の方が陰性が強いということは、善玉は正常なタンパク膜にくっつきにくい・・・ということになります。
でも膜が劣化してプラスに変わったらくっつきます。
そして、以下は間逆です。
『脂質異常症(高脂血症)』より引用
LDLはプラスに荷電している。
一方、平滑筋細胞や内皮細胞において産生される糖タンパクであるプロテオグリカンはかなり強くマイナスに荷電している(プロテオグリカンは細胞外基質である)。
プラスに荷電したLDLがマイナスに荷電したプロテオグリカン(糖鎖の部位)に引き付けられるように強固に結合すると、LDLの構成タンパクであるApo-Bタンパクは構造変化して血管壁から外へ出ることはない。
なんと、いきなり「LDLはプラスに荷電している」・・・ときました。
そうすると「正常なタンパク膜(ほどんどゼロ)」の時より、「劣化したタンパク膜(プラス)」の時の方が反発してよりくっつきにくくなる気がします。
しかし、ちょっと気になったのが、以下の部分です。
>平滑筋細胞や内皮細胞において産生される糖タンパクであるプロテオグリカンはかなり強くマイナスに荷電している(プロテオグリカンは細胞外基質である)。
「プロテオグリカン」・・・
内皮細胞の上にある「たんぱく成分の膜」膜は、「グリコサミノグリカンス、糖タンパクで出来た膜」と説明がありました。
一応「グルコサミノグリカンス」と「プロテオグリカン」について調べてみました。
グリコサミノグリカン(glycosaminoglycan)は、長鎖の通常枝分れがみられない多糖。動物の結合組織を中心にあらゆる組織に普遍的に存在する。狭義のムコ多糖。GAGと略される。
硫酸基が付加した2糖の繰り返し構造からなる。
うち1つはアミノ糖(ガラクトサミン、グルコサミン)であり、もう1つはウロン酸(グルクロン酸、イズロン酸)またはガラクトースである。
多数の硫酸基とカルボキシル基を持つために、強く負に帯電している。
多くのグリコサミノグリカンは、プロテオグリカンとしてコアタンパク質と呼ばれる核となるタンパク質に付加した形で存在している。唯一の例外は、ヒアルロン酸であり、プロテオグリカンとしては存在していない。
「グルコサミノグリカンス」は強く負に帯電しているとのことです。
プロテオグリカンは、動物成分の多糖類(グリコサミノグリカン:glycosaminoglycan)の研究中に見つけ出された成分である。
グリコサミノグリカンとしては、ヒアルロン酸や軟骨から分離されたコンドロイチン硫酸(1889)などが有名であるが、これらのグリコサミノグリカンの構造解析を行っている中で、1970年にグリコサミノグリカンとコアタンパク質(CoreProtein)が一定の結合様式で結合した糖タンパク質が発見され、プロテオグリカンと命名された。
イマイチ何が言いたいのかよく分からない説明ですが、
グルコサミノグリカン + タンパク質 = プロテオグリカン
・・・ということなので、「プロテオグリカン」とは、「タンパク膜」のことを指しているのでしょう。ハッキリ「膜」と言えばいいのにと思います。
それを踏まえた上で、以下の部分をもう一度読みます。
>平滑筋細胞や内皮細胞において産生される糖タンパクであるプロテオグリカンはかなり強くマイナスに荷電している(プロテオグリカンは細胞外基質である)。
「グルコサミノグリカン」が強く負に帯電しているので、この「プロテオグリカン」は強くマイナス・・・ということだと思うのですが、
そうすると、最初に紹介した「グルコサミノグリカンスと糖タンパクでできているタンパク膜は、電気的にほとんどゼロ」という話と食い違います。
混乱してきたので図にします。
「正常な膜」を「ほとんどゼロ」から「マイナス」に、血液中の成分の中の「LDLコレステロール」だけを「マイナス」から「プラス」に変えると、
「血液中の成分」と「タンパク成分の膜」がくっつくか、くっつかないかの話が、先ほどと違ってきます。
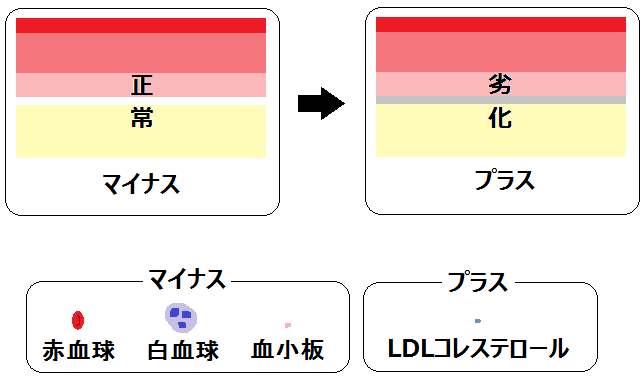
仮に正常な「タンパク膜」が強いマイナスと過程して、さらに、「LDLコレステロール」もプラスと仮定したら、「LDLコレステロール」と正常な「タンパク膜」はくっつきます。
でも、「タンパク膜」が劣化してプラスになれば、「LDLがコレステロール」がプラスだった場合は反発することになります。
膜が傷ついていても「LDLコレステロール」が中に入りにくいことになります。
どっちが本当なのかよく分からないですね。
検証のしようがないので、とりあえず「電荷」の件は保留にします。
スポンサーリンク
カルシウムによる石灰化
タンパク成分の膜が壊れると問題が起こります。
その一つが、組織の「石灰化」です。
もう一つ、ここでたいへん興味深い現象が起きることがあります。台風などで河川の堤防が決壊すると、そのときは本格的な修理をしている余裕などはありませんから、応急処置として破壊された部分に砂袋などを積み重ねます。
実はこれと似たようなことが動脈の組織で起きるのです。
タンパク膜の質が悪くなって動脈壁が栄養不足に陥ると、組織を構成している重要な成分であるエラスチンやコラーゲンの新陳代謝も低下し、作り替えが行なわれなくなって、やがては壊れて量が減ってきます。すると、組織はあわてて手近にある他の材料で代用して、このすき間を埋めようとするのです。
その代用品がカルシウムです。
血液中のカルシウムイオンが組織内にとり込まれて、リン酸カルシウムとなり、エラスチンやコラーゲンがあった場所を埋めるのに使われてしまいます。動脈硬化が進行すると、組織の石灰化(リン酸カルシウムの沈着)が見られるのは、こうした理由からなのです(146ページ・図24―②参照)。
このように、動脈硬化が起きるそもそもの原因は、動脈壁内外に存在するタンパク膜の形態や機能が悪くなることにほかなりません。
動脈硬化を引き起こす“主役”はこのタンパク膜の変性や破壊であり、コレステロールやカルシウムも関係はしていますが、あくまでも途中から加わる“脇役”にすぎないのです。
タンパク膜の変性がなぜ起きるのかについては現在研究中ですが、遺伝的素因にさまざまな要因が加わって生じるものと思われます。
したがって、血中のコレステロール濃度がどんなに高くても、膜が正常である限り動脈硬化は発生せず、LDLコレステロールが動脈壁にくっついたり侵入したりすることもありません。逆に血中のコレステロール濃度が低くても、膜の質が悪くなれば動脈硬化は発生し、LDLコレステロールも動脈壁にくっついたり侵入したりするのです。
これは、高脂血症でも動脈硬化を起こさない例がたくさんあり、逆にコレステロール値が低くても動脈硬化を起こす人が非常に多いという、これまでに多くの臨床研究で得られている結果とも一致しています。
(151~158p)
動脈硬化の原因ですが、
>動脈硬化を引き起こす“主役”はこのタンパク膜の変性や破壊であり、コレステロールやカルシウムも関係はしていますが、あくまでも途中から加わる“脇役”にすぎないのです。
とあります。
これが答えです。
つまり、動脈硬化を根本的に防ぐには、タンパク膜の変性や破壊を防がなければならないというわけです。カルシウム対策は二の次ということです。
しかし、
>タンパク膜の変性がなぜ起きるのかについては現在研究中ですが
・・・とあるように、「変性の具体的な原因」までは、この時点で判明していないようです。
先ほども言ったように、ネットや本で調べても、書かれているのは、文章、イラスト共に動脈壁の「内皮細胞」までで、その上の「タンパク膜」について触れられていません。
そして、動脈硬化の説明は、「膜が壊れたところ」からスタートしているので、膜が変性する具体的な理由も見つかりませんでした。
「タバコ」、「ストレス」、「老化」、「何らかの原因で...」・・・とかなり曖昧です。
なので、私が「タンパク膜」が変性してしまう理由についてお話します。
スポンサーリンク
タンパク質の変性
タンパク質はデリケートな分子です。従って、何かの「影響」によって、立体構造が変化し、性質が変わってしまうのです。
これを「タンパク質の変性」と言います。
「影響」とは、例えば、加熱、攪拌、酸、アルカリ、尿素などです。
そして、「糖質」もタンパク質を変性させます。これを「糖化反応」と言います。
変性の原因の中でも大きいのが「糖化反応による変性」です。その理由は、あらゆる有害物質の中で「糖質」が最も取り込む量が多いからです。
「糖質」は血管に炎症を起こす原因にもなりますが、体のタンパク質を変性させる原因にもなります。
で、「タンパク成分の膜」ですから、当然糖化対象でしょう。さらに言えば「エラスチン」と「コラーゲン」と「細胞」もタンパク質ですから、糖化対象です。
糖質をバクバク食べていれば、血管を構成するタンパク質は糖化します。
だから、動脈硬化ではなく「動脈糖化」です。
私は長年糖質過多だったので、糖化によって体がボロボロになりました。その為、多くの人に糖化の危険性について知ってもらいたいと思っているのですが、現代の医療関係者でも「糖化」にはほとんど触れません。
この本が出版された1998年は、「糖化」という概念は広がっていませんでした。だから、「タンパク膜」が変性する可能性として「糖化」は考え付かなかったのだと思います。
しかし、この本に「糖化」という単語はでてきませんが、それを思わせる記述がいくつも書いてありました。
「糖化によって「タンパク膜」が変性破壊された」・・・と考えれば整合性がとれます。
糖質を大量に食べている人なら、「糖化」が起きても不思議ではないのです。
「糖化反応」は血管だけに起こるわけではありません。関節、肌、内臓、卵子・・・等、全身に起こります。症状は一見「老化」に似ています。具体的にどうなるか知りたい方は以下の記事をお読み下さい。
ちなみに血液検査で測る「ヘモグロビンA1c」ですが、あれは、タンパク質である「ヘモグロビン」に糖がどれぐらいくっついているかを測っているのです。糖質は、血管だけでなく、血液成分にも影響を与えるのです。
動脈硬化の対策
動脈硬化の一番の予防は、体のタンパク質を変性させたり、炎症の原因になる「糖質」を控えることです。
その上で、既にバリア機能のあるタンパク膜が壊れている人は、「小型LDLコレステロール」を減らす努力も必要です。
「酸化」と「糖化」を防ぐ為に...
AGEは2つの仕組みで、アテロームによる動脈硬化を進行させます。
動脈硬化の最初の引き金になるのは、血液中に増えすぎた悪玉コレステロールの血管への蓄積です。
血管に蓄積した悪玉コレステロールは、AGEによる悪玉修飾を受けます。悪玉修飾を受けた悪玉コレステロールは、処理をするために出動したマクロファージに摂り込まれて「泡沫細胞」となります。この泡沫細胞がアテロームをつくったり、動脈の内側を厚くしたりするのです。これが第1の仕組みです。
もう1つ、AGEには血管に対する直接的な悪影響もあります。
血管の内側にある「血管内皮細胞」には、AGEをキャッチするアンテナ(受容体)があります。この受容体にAGEが結合すると、動脈硬化を進め炎症反応がおこります。
そして、もう一つ大事なことがあります。
それは、タンパク質を増やす事です。その根拠が以下になります。
ご存じのように、生体の臓器や器官はすべてタンパク質でできていますが、このタンパク質を合成しているのは臓器や器官に存在する細胞です。
動脈壁の組織においても、細胞は栄養呼吸によってとり入れられた栄養分に養われながらタンパク質を合成し、日々新陳代謝を営んでいます。
血管の構造や機能を正常に保つためには、こうした細胞による新しいタンパク質の合成が活発に行なわれ、老化や障害を起こしたタンパク質との交換がきちんと行なわれていることが必要です。
さらに注目すべきなのは、栄養呼吸をつかさどっている動脈壁内外のタンパク膜自体も動脈壁の細胞によって合成されているという点です。
動脈硬化を防ぐためには、このタンパク膜の新陳代謝がスムーズに行なわれ、常にリフレッシュされていることがいちばん重要となります。
(179~180p)
タンパク質は体の材料なので、体の修復の為には、絶対必要です。
今回紹介した長谷川氏の本ですが、1998年の時点で、コレステロールと動脈硬化は関係ない事、糖質を減らした方が良い事を述べられています。
それだけでなく、中高年が肉を減らすのは大間違い、タンパク質+脂質の割合を50%ぐらいにはした方が良いとも言われています。
当時の私が読んだら「何言ってんの?」と思ったでしょうが、今考えると糖質制限の概念もなかったこの時代に、このような主張をするのは凄いと思います。
長谷川氏は、血管を研究する人なので、動脈硬化の「血管の状態」を詳しく述べられていてとても参考になりました。
現在、動脈硬化を研究している学者には、大きく分けて三つのグループがあります。
一つは、主に血液を研究しているグループで、簡単にいうと、血液中に含まれる成分やその作用などを明らかにすることによって、動脈硬化の原因を突き止めようとしています。
血液に含まれる成分を研究するのがいわば本職で、得意分野ですから、その成分の一つである血中コレステロールに注目しがちな傾向があります。「コレステロール元凶説」を唱える学者の多くは、このグループの人たちです。
二つ目は、血管壁の表面の細胞(内皮細胞)や組織内の細胞(平滑筋細胞)をとり出して培養し、その生態や病態を観察・研究するグループです。
ただし、この場合も主としてウサギの細胞を実験の対象としており、病態をつくり出すためにはコレステロールなどを負荷する方法が用いられます。結局は、一つ目のグループの研究と連動していることが多く、「コレステロール元凶説」を裏づけることをその研究の目的としていると言ってよいでしょう。
三つ目は、主に血管そのものを研究しているグループです。血管を構成している材料、血管の状態や働きなどを検討することによって、動脈硬化の原因をさぐっていきます。私自身はこちらのグループに入るでしょう。
問題は、現状では前の二つのグループのほうが圧倒的に人数が多いということです。
血液研究グループ+細胞培養研究グループが9・5に対して、血管研究グループは0・5ぐらいの割合でしょうか。
そのため、どうしても血液研究グループや細胞培養研究グループのほうが力も強く、声も大きくなりがちで、「コレステロール元凶説」が有力になったという背景もあるのです。
(43~44p)
20年近く経っているので、現在の状況は分かりませんが、貴重な、血管そのものを研究しているグループに属する人の意見です。
長くなるので、最初は要約しようかと思ったのですが、私が分かったような事を言うよりも、直接血管を観察している人の主張をそのまま紹介した方が説得力があるので、引用をメインにしました。
改めて動脈硬化の原因について考える
本気で動脈硬化を避けたいのであれば、血管を傷つけない事、その原因になる糖質の量に気をつけることです。
しかし、動脈硬化の原因を探していると、内皮細胞が傷つくのは、高血圧、糖尿病、喫煙、ストレス・・・とサラッと流し、コレステロールの小難しい話に突入します。判で押したようにこのパターンが多いです。
コレステロールが悪い
↓
悪玉LDLが悪い
↓
小型LDLが悪い
・・・と、コレステロールに関しては細かい話をするくせに、肝心なところにダメージを与えるであろう「糖質が与える影響」についてはほぼ無視です。
糖尿病、高血圧・・・ときたら、もう一歩踏み込んで「糖質」をあげないとおかしいわけです。コレステロールを追求する時の勢いと違います。
コレステロールを下げる薬を飲んでいる人は多いようですが、根本的な原因である血管を傷つける糖質をバクバク食べていたら、血管はボロボロになります。
スポンサーリンク