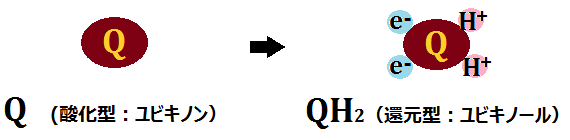- 投稿 2017/12/14
- 分かりやすいシリーズ

電子伝達系の後半になります。前半は以下です。
電子伝達系(呼吸鎖)について分かりやすく説明してみた①複合体Ⅰ~Ⅱ
前半でも少しお話しましたが、「電子伝達系」の説明は情報源によってバラバラです。
簡単な生化学の本ではだいたい同じような説明になっていますが、さらに一歩踏み込んで調べようとすると、非常に複雑で、どの情報も言っている事が微妙に違います。そんなのネットだけだろ、と思われるかもしれませんが、本もです。
今回、調べた情報をまとめて、だいたいの流れを書きましたが、元ネタがそのような状態なので、私としても半信半疑です。
調べれば調べる程、納得のいかない事がでてくるので、何回書き直したか分かりません。
もっと時間をかけて調べて、完全に分かってから記事を公開しようと思っていたのですが、気が済むまで調べ始めると何時公開できるか分かりません。従って、今後修正するという前提で、現時点でまとめた事を公開することにしたのです。
なので、本記事の説明は、あくまで現在言われている説の1つだという感じで捕らえるようにして下さい。
それでは、続きの「複合体Ⅲ」から説明します。
スポンサーリンク
③ユビキノール:シトクロムcレクターゼ複合体(複合体Ⅲ)
「複合体Ⅰ」や「複合体Ⅱ」から離れた「ユビキノール」は、「ユビキノール:シトクロムcレクターゼ複合体(複合体Ⅲ)」に到着します。
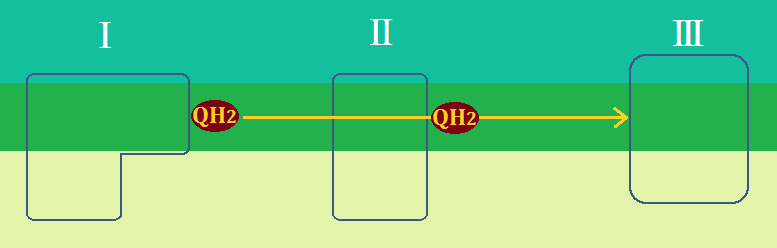
「複合体Ⅲ」は、「複合体Ⅰ」や「複合体Ⅱ」から生じたユビキノールの電子を「シトクロムc」に伝達する役割と、
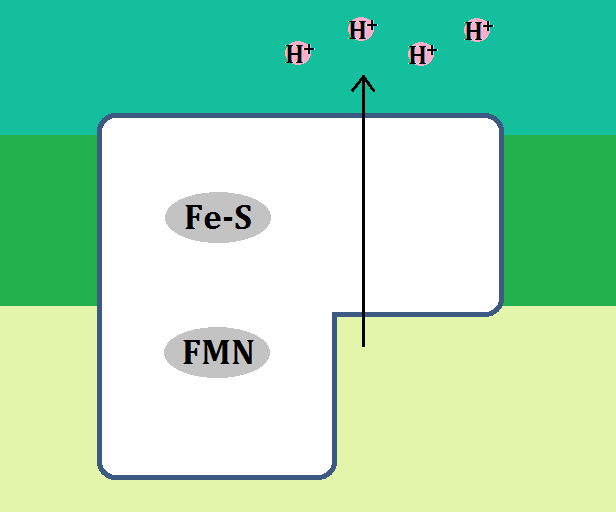
マトリックスの「H+」を、膜間腔に放出する役割があります。
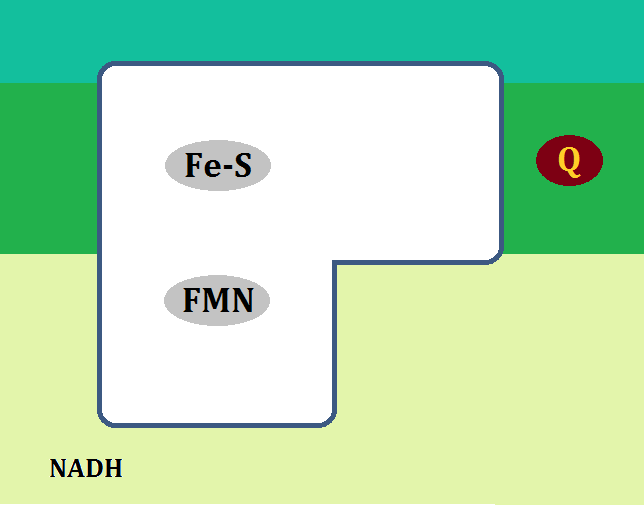
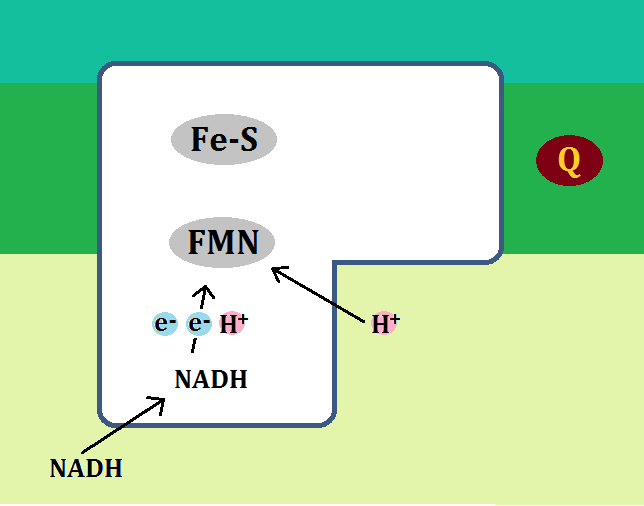
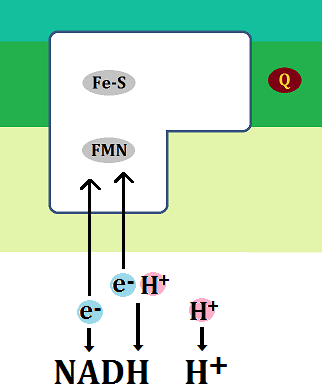
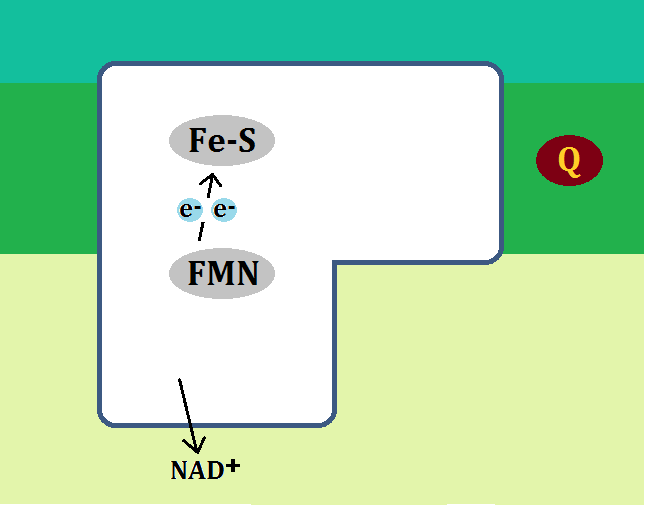
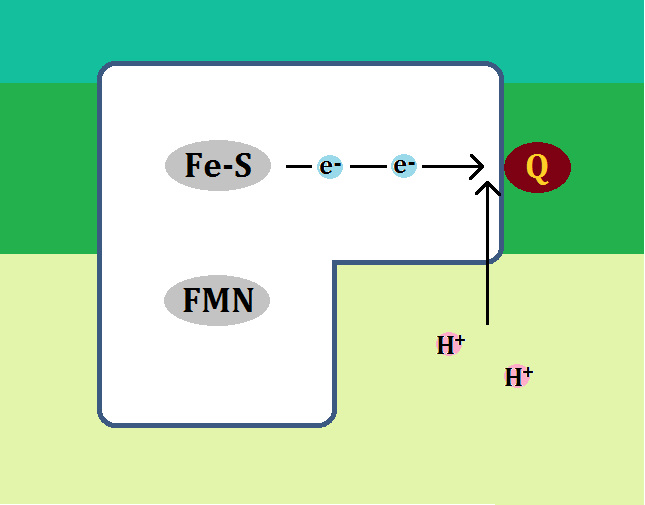
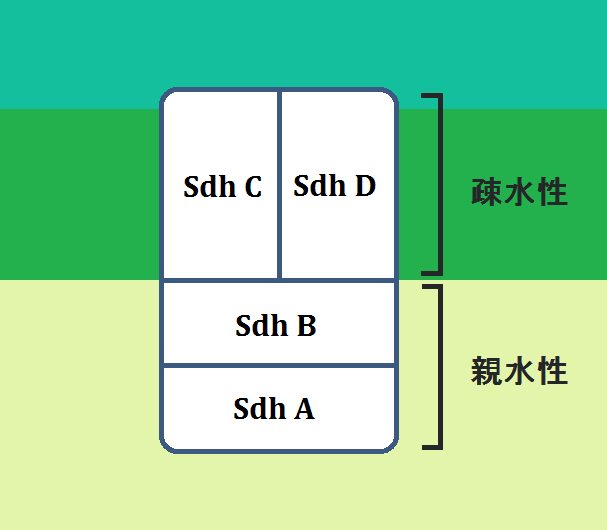
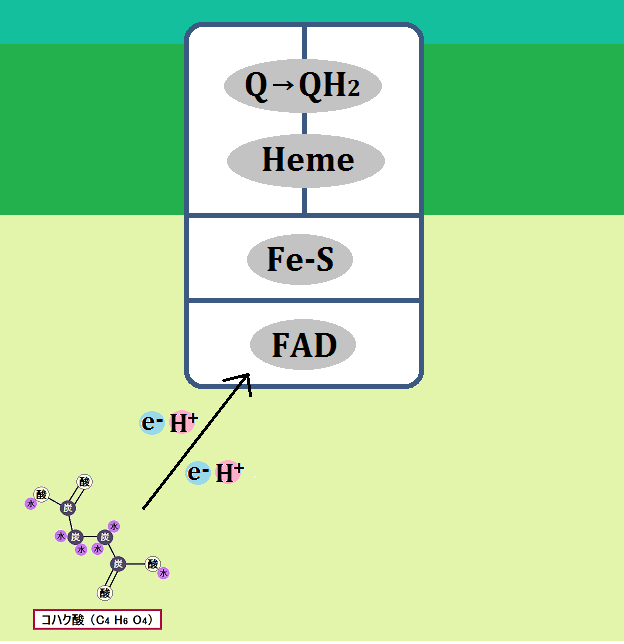
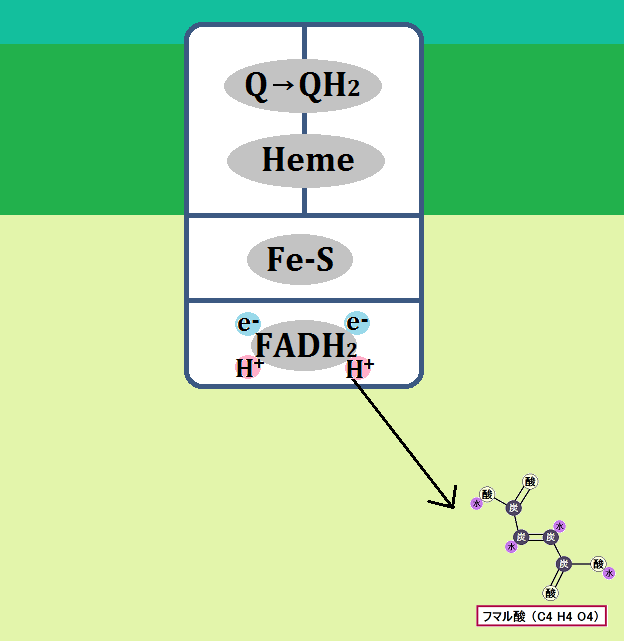
構造はこのようになっています。
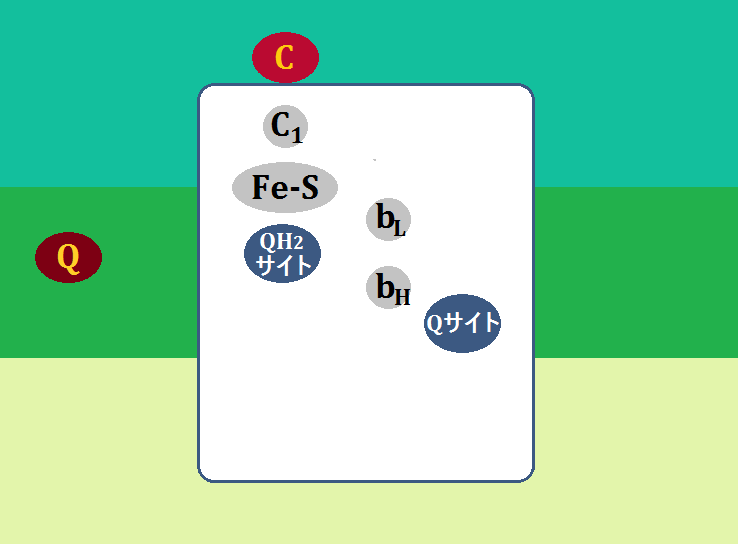
「シトクロムc」や「Fe-S(鉄硫黄クラスター)」については、前半でお話しました。
「QH2サイト」は、ユビキノールを受け入れる所、「Qサイト」はユビキノンやセミキノンを受け入れる所です(※セミキノンは後で説明します)。
「bL」と「bH」は、ヘムタンパク質で、「シトクロムb」と言います。「bL」のことを「b562」、「bH」のことを「b566」と表記しているものもあります。
それでは、話を戻します。
この「複合体Ⅲ」での電子のやり取りは、2段階です。
まずはステップ1です。
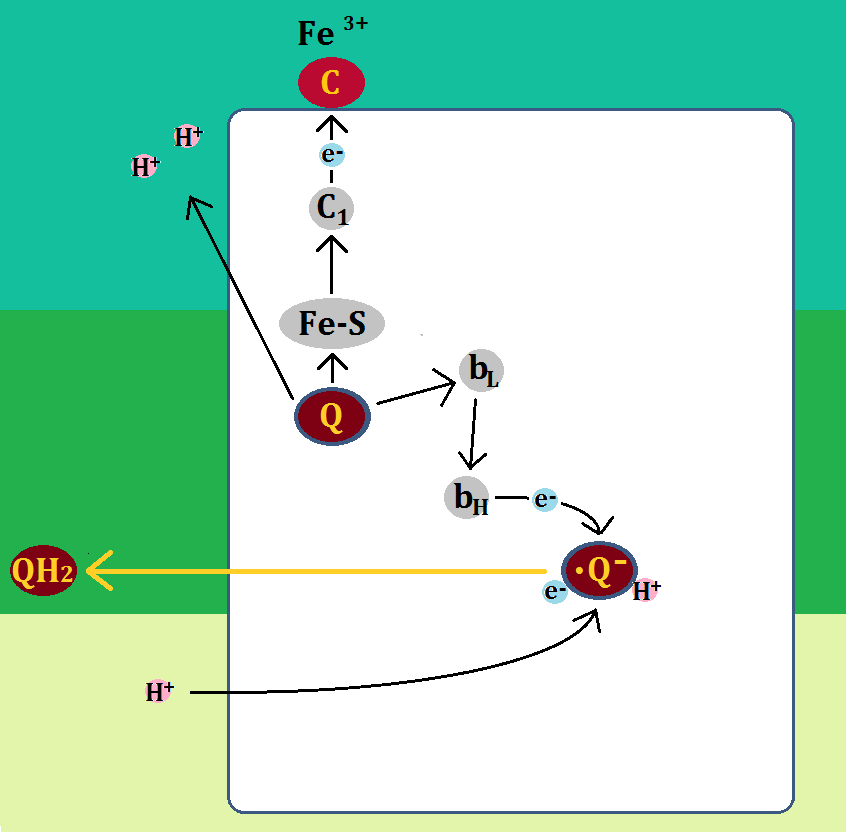
複合体ⅠやⅡから来た「ユビキノール(QH2)」は、複合体Ⅲの「QH2サイト」に結合します。
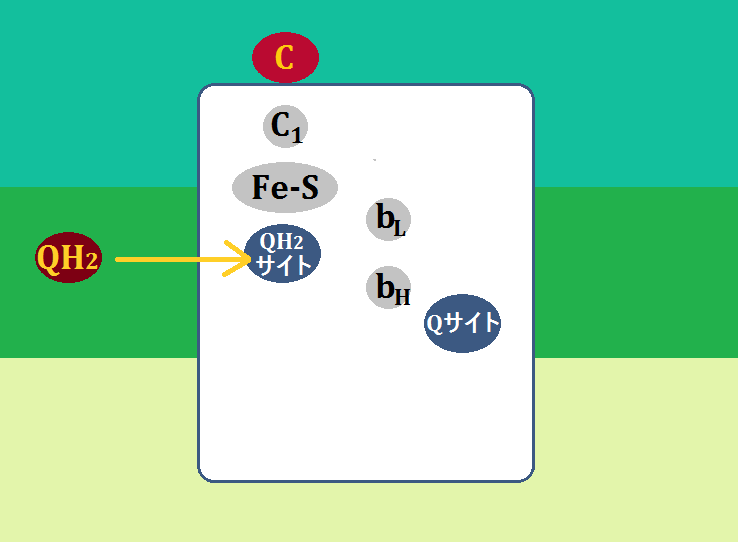
「ユビキノール(QH2)」は、電子(e+)を2つ、水素イオン(H+)2つを運んできたわけですが、「電子」の1つを「Fe-S」に、もう1つを「bL」に渡します。
そして、残った「水素イオン」2つは膜間腔に放り出されます。
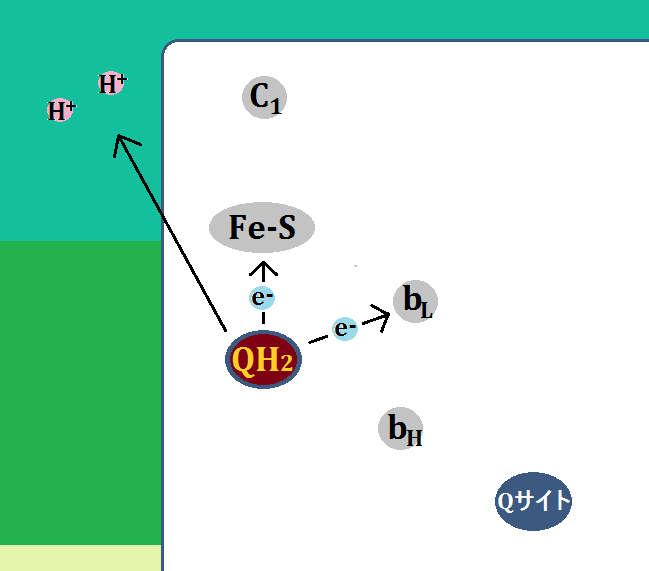
「QH2(ユビキノール)」は水素を失ったので、酸化型の「Q(ユビキノン)」になります。
その後、ユビキノンは、「Qサイト」へ移動します。
そして、「bL」に移動した電子は、「bH」を経て「Qサイト」に結合した「Q(ユビキノン)」に渡されます。
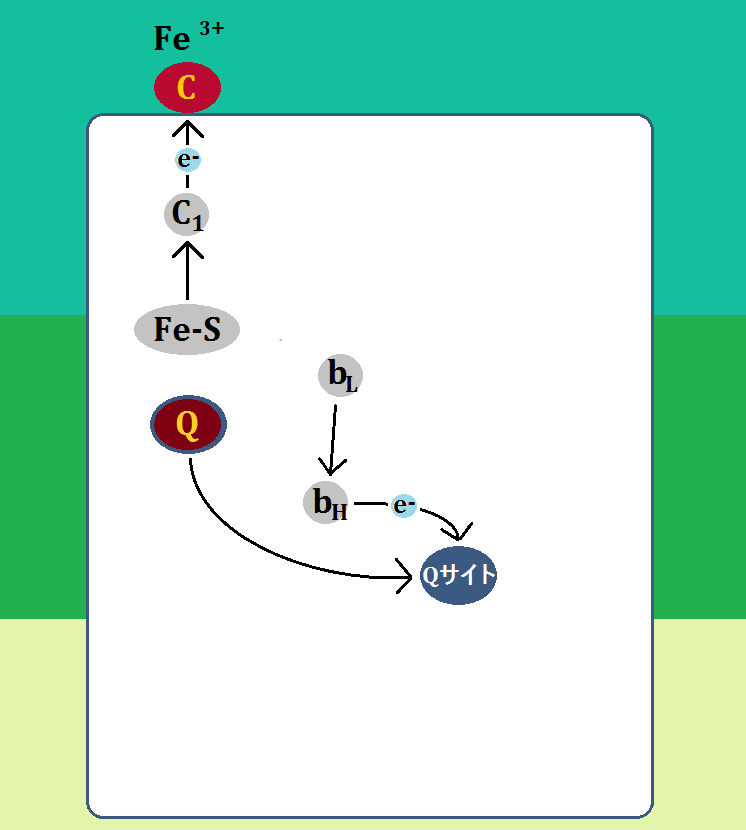
「ユビキノール」から「Fe-S」に移動した電子は、「シトクロムc1」を経て、独立したヘムタンパク質である「シトクロムc(酸化型Fe3+)」に渡されます。
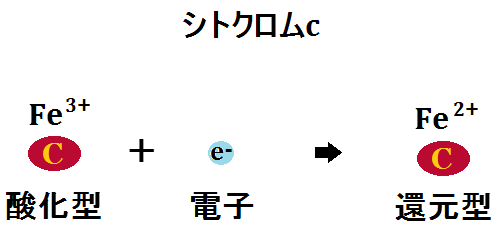
「シトクロムc」は、電子を受け取ることで「還元型(Fe2+)」となり、複合体Ⅲを去ります。
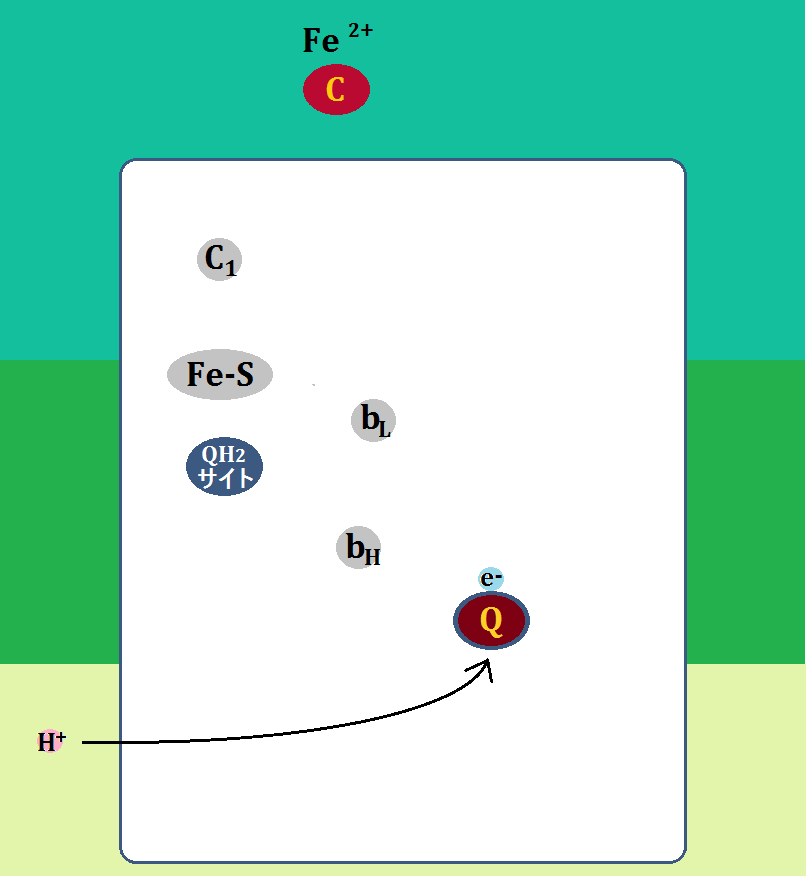
電子を1つもらった「Q(ユビキノン)」は、マトリックス側から「水素イオン(H+)」を取って「・Q-(セミキノン)」となります。
「ユビキノン」に2つの水素がつくと「ユビキノール」ですが、1つの水素がつくと「セミキノン(ユビセミキノン)」です。
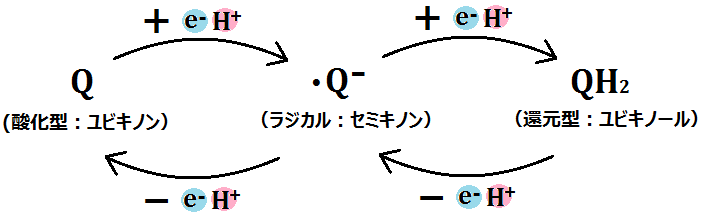
ここまでが「複合体Ⅲ」の第一段階です。まだ終わりではありません。
ここからはステップ2です。
次に、また別の「QH2」が「QH2サイト」に結合します。
そして、ステップ1と同じように、「QH2」は電子を「Fe-S → シトクロムc1 → シトクロムc」と渡し、シトクロムcを還元型にします。
同じく「H+」は膜間腔に放り出されます。
そして、「ユビキノール(QH2)」は、「ユビキノン(Q)」になります
そして、もう1つの電子は「bL → bH → ステップ1によって生じたセミキノン」に渡されます。
電子を得た「セミキノン」は、マトリックスから「H+」を取り込み、還元型の「ユビキノール(QH2)」になって、複合体Ⅲを出て行きます。
これで「複合体Ⅲ」の流れは終わりです。
しかし、もう1つ別の説も紹介します。もちろん、どちらが正しいかは分かりません。こちらもステップ1と2に分けて説明します。
では、別の説のステップ1です。
まず最初に、「QH2」が「QH2サイト」に結合します。そして、電子(e-)を「Fe-S」と「bL」に1つずつ渡し、残った水素イオン(H+)を膜間腔に放り出します。
ここまでは同じで、違うのはここからです。
電子と水素イオンを渡した「ユビキノール」は還元型の「ユビキノン」になるのですが、「QHサイト」から「Qサイト」へ移動しません。
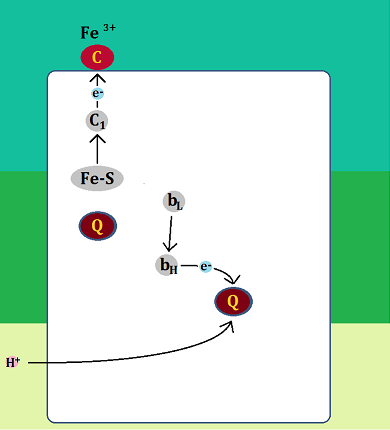
そして、「bL」が受け取った電子は、「bH」を経て、別の「ユビキノン」に渡されます。
電子を受け取った「ユビキノン」は、マトリックスから「水素イオン(H+)」を1つ取り込んで「セミキノン」になります。
一方、「Fe-S」が受け取った電子は、「シトクロムc1」を経て、「シトクロムc」に渡されます。「シトクロムc」は還元型(Fe2+)になります。
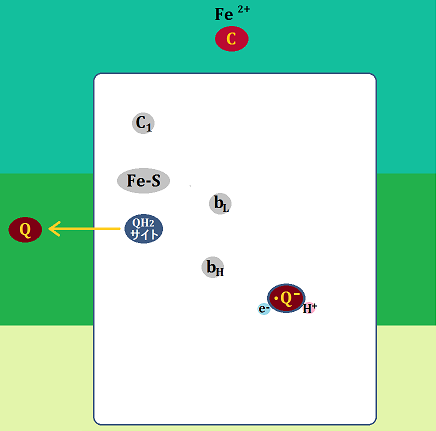
そして、「QH2サイト」にいた「ユビキノン」と、還元型になった「シトクロムc」は複合体Ⅲを去ります。
「セミキノン」は「Qサイト」に留まります。
ここからステップ2です。
別の「QH2」がやってきて、電子を「Fe-S」と、「bL」に渡し、水素イオンを膜間腔に放りだします。
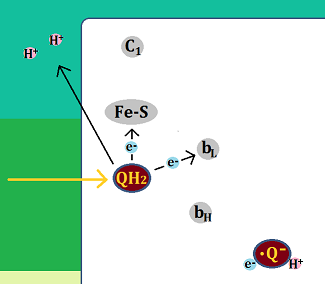
「Fe-S」に渡された電子は、「シトクロムc1」を経て、「シトクロムc」へ、
「bL」に渡された電子は、「bH」を経て、ステップ1で生じた「セミキノン」へ渡されます。
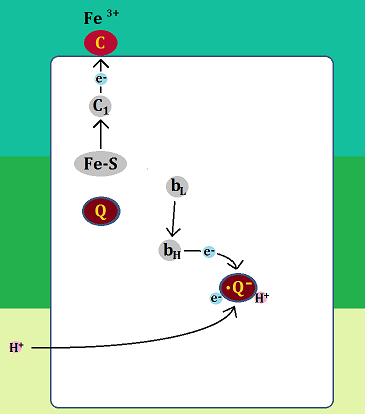
「セミキノン」はマトリックスから「水素イオン(H+)」を取り込んで「ユビキノール」になります。
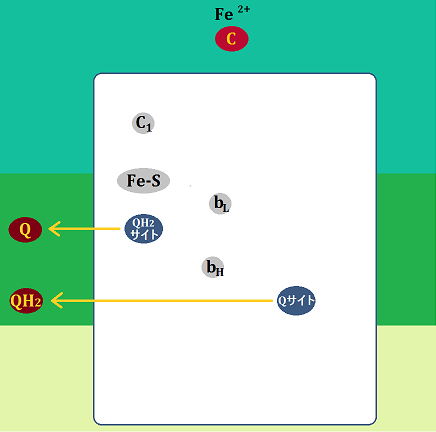
還元型になった「シトクロムc(Fe2+)」と、
「QH2サイト」にいた「ユビキノン(Q)」と、「Qサイト」の「ユビキノール(QH2)」は、複合体Ⅲを離れます。
以上が複合体Ⅲの流れになりますが、このように情報がハッキリしないので大まかな流れだけ覚えるようにした方がよさそうです。
スポンサーリンク
④シトクロムcオキシターゼ複合体(複合体Ⅳ)
複合体Ⅲを離れた還元型の「シトクロムc」は、電子伝達系の最後である「シトクロムcオキシターゼ複合体(複合体Ⅳ)」に辿り着きます。
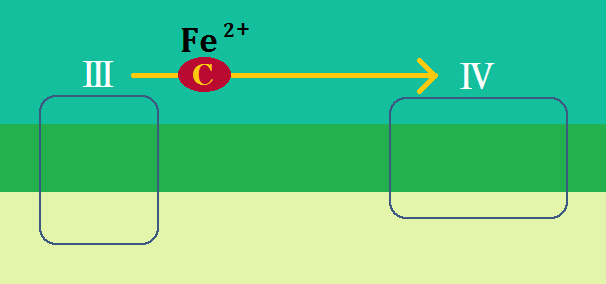
この複合体Ⅳは、シトクロムCから電子を預かって酸化型のシトクロムcにし、
電子を酸素(O2)に渡して、水素イオンも取り込み、水(H2O)を生成します。
「複合体Ⅳ」は、13個のサブユニットから構成されているとのことなのですが、酵素活性の機能的な中核となるのは「サブユニットⅠ」と「サブユニットⅡ」だそうで、調べてみると以下のようにサブユニットⅠ~Ⅲまでを描いている画像が多かったです。
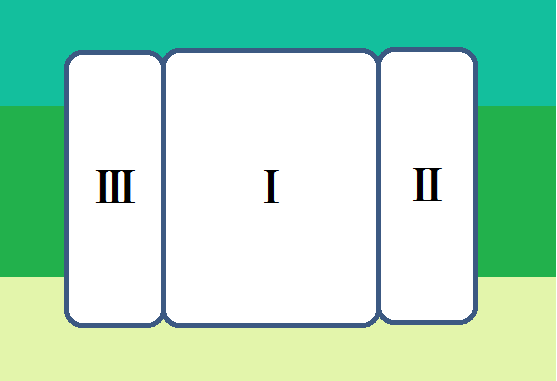
で、機能的な中核であるⅠとⅡは、このようになっています。
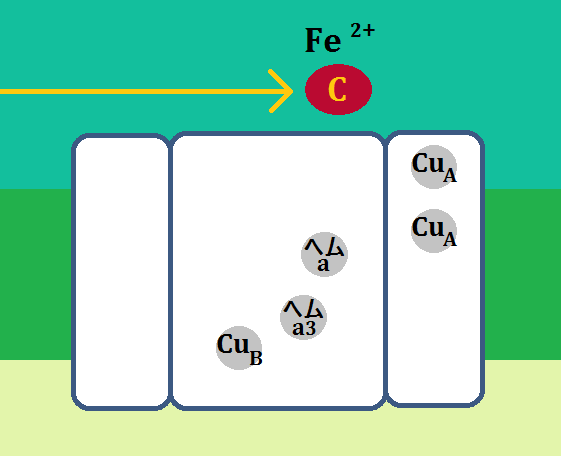
「サブユニットⅠ」に2つあるのは、「CuA」です。「Cu」は胴です。
「サブユニットⅡ」には、2種類のヘム、「ヘムa」と「ヘムa3」、
そして、「CuB」があります。
流れはこうです。
「シトクロムc」が「複合体Ⅳ」に到着すると、電子は「CuA」に移動します。その後、電子は「CuA」、「ヘムa」、「ヘムa3」、「CuB」と移動していきます。
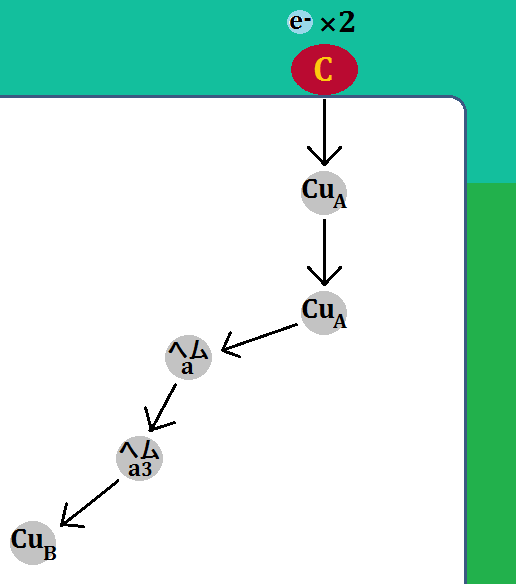
電子を伝達した「シトクロムc」は酸化型の「Fe3+」に戻り、「複合体Ⅳ」を離れます。
その後、また還元型の「Fe2+」が電子をつれてやってきます。そして、同じように電子を伝達します。
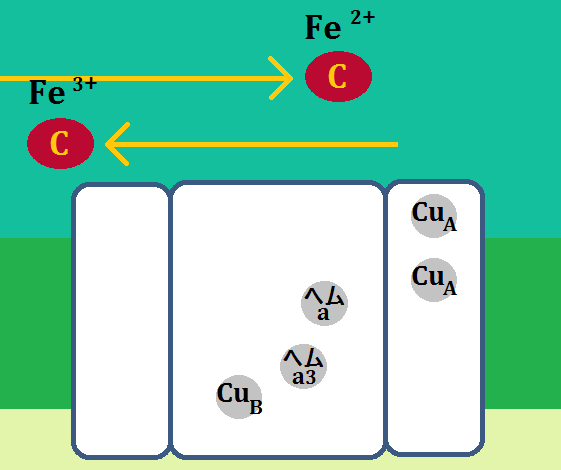
電子2回分によって、「ヘムa3 (Fe3+)」と、「CuB (Cu2+)」が還元されます(※Feは鉄です)。
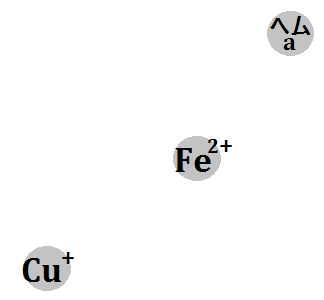
●(Fe3+) → 還元 → (Fe2+)
●(Cu2+) → 還元 → (Cu+)
それによって、「酸素分子」が結合できるようになります。
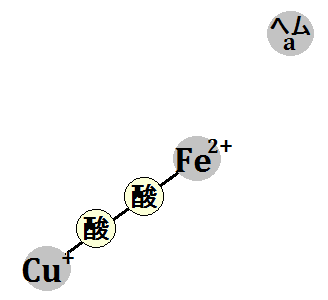
すると、酸素はその電子を受け取ります。
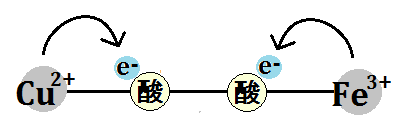
「酸素分子」はさらに電子を2つ受け取り、マトリックスから水素イオンも取り込みます。
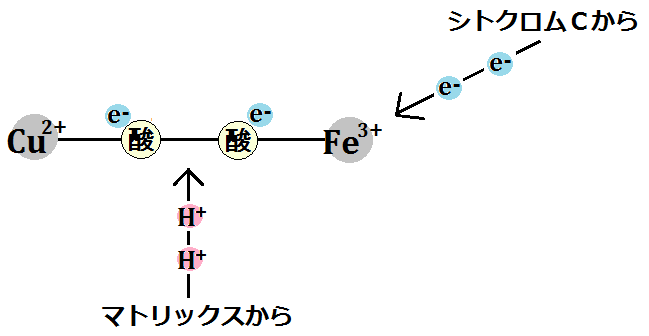
すると、結合もなくなります。ここまで「酸素分子」が手に入れたのはこれだけです。
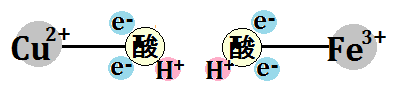
そして、「水素イオン(H+)」を2つ取り込みます。
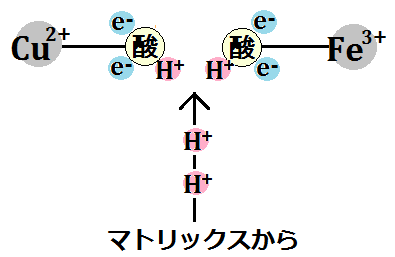
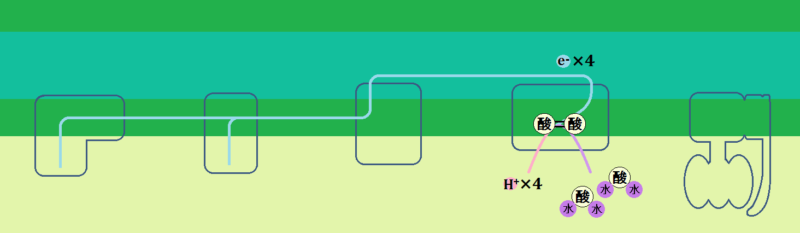
「O2」は、シトクロムcから「電子(e-)」4つと、ミトコンドリアのマトリックスから、「水素イオン(H+)」4つ受け取ったことになります。

それで、2分子の水が生成されます。
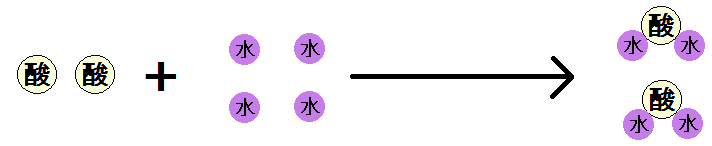
電子の伝達はこれで終了です。
「ミトコンドリアでの代謝には酸素が必要」と言われるのは、内膜の「電子伝達系」の最後で、電子の受け取り手である「酸素」が必要だからです。
で、この酸素が水分子になるまでの流れは、別の説もあります。一応紹介しておきます。
酸素が電子2つによって還元されるところまでは同じです。
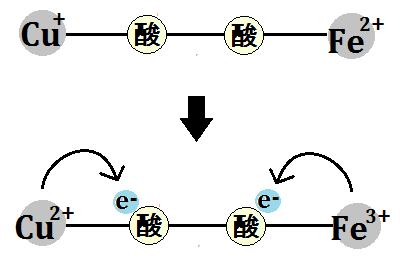
3つめの電子が1つ取り込まれて、水素イオンも1つ取り込まれます。
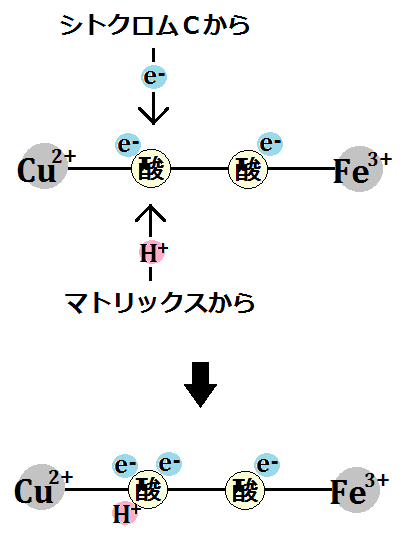
そして、4つめの電子が1つ取り込まれて、水素イオンも1つ取り込まれます。その後結合が切れます。
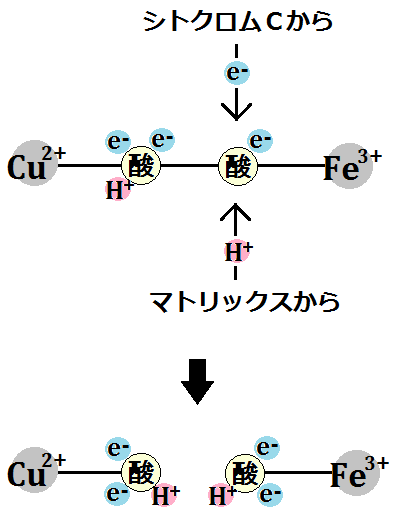
後は水素イオンを2つもらうので同じです。
細かい違いなので、「酸素に電子4つと、水素イオン4つが結びついて水分子になる」というところだけ覚えておくとよいでしょう。
ところで、水を生成する為に、マトリックスから「水素イオン(H+)」が4つ取り込まれたわけですが、
複合体Ⅳでは、これとは別に4つの「H+」が取り込まれ、膜間腔に放り出されます。
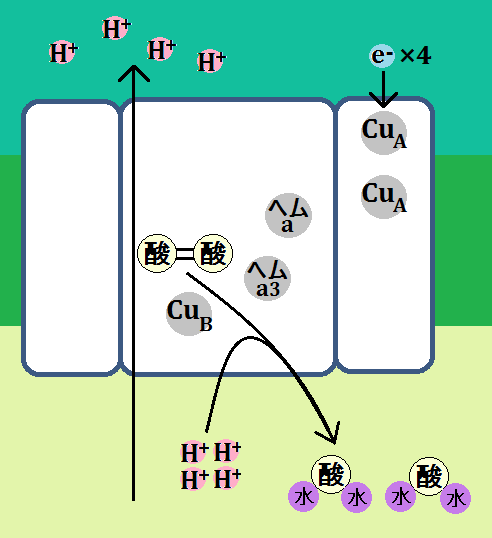
「電子」の伝達は終わりましたが、まだ膜間腔に放り出された「水素イオン(H+)」と、5つ目の複合体である「ATP合成酵素」が残っています。
スポンサーリンク
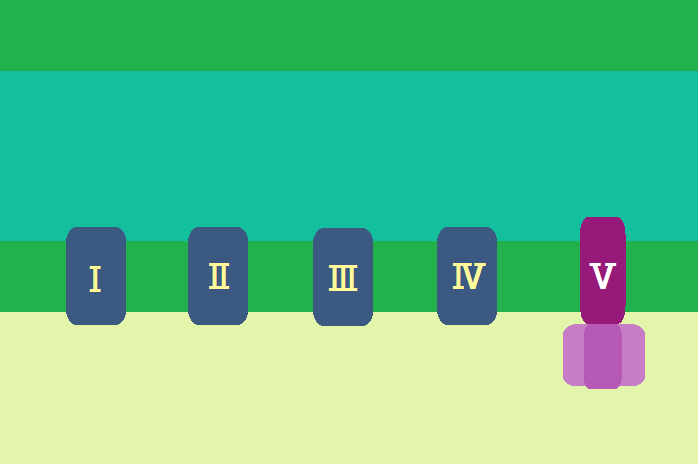
⑤ATP合成酵素(複合体Ⅴ)と酸化的リン酸化
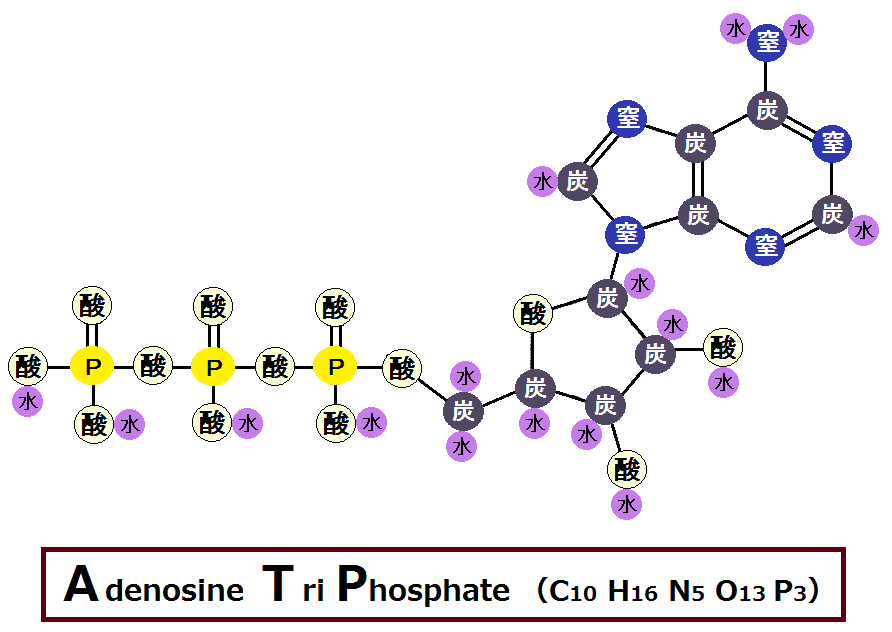
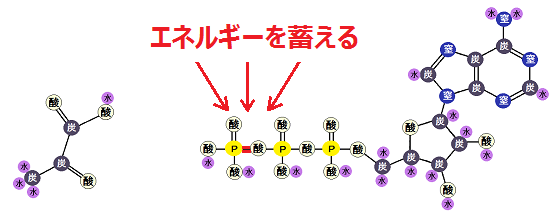
「電子伝達系」の目的はATPを作ることです。
ここからは、内膜でどのようにして「ATP」が合成されるのか説明していきます。
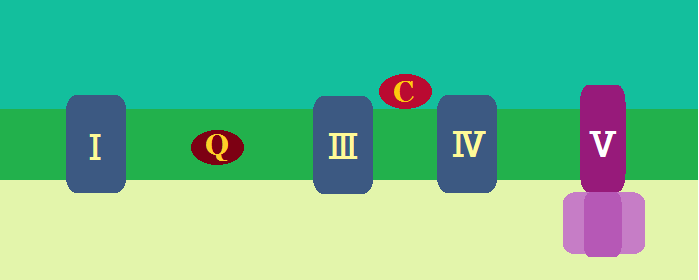
複合体Ⅰ~Ⅳの間を電子が渡っていくエネルギーで汲み出された「水素イオン(H+)」は、やがて膜間腔の中で溢れ、マトリックス側より「H+」の濃度が濃くなります。
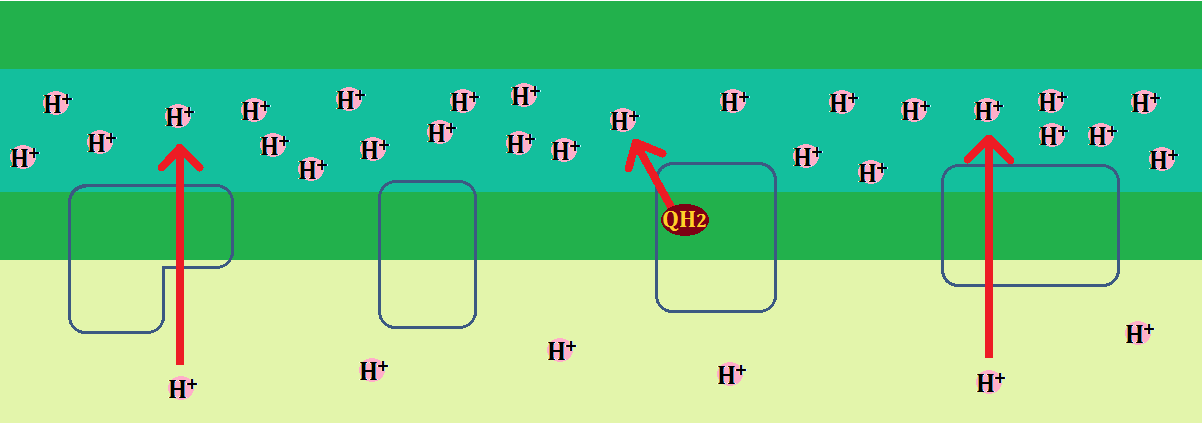
ここで思い出してほしいのが水力発電です。
水力発電は、ダムに溜めた水が流れる力でタービンを回して発電します。その仕組みと「ATP合成酵素」は良く似ていて、膜間腔に溜まった「H+」がマトリックスに流れる力を利用して、「ADP」と「リン酸」から「ATP」を作ります。
これを「酸化的リン酸化 さんかてきりんさんか」と言います。
ただし、基本的に内膜は「水素イオン(H+)」を通さないので、どこからでもマトリックスに戻れるわけではありません。
「H+」がマトリックスに戻る道が、5つ目の複合体「ATP合成酵素(複合体Ⅴ)」で、タービンに相当するものがついています。
従って、「世界最小のモーター」と言われています。
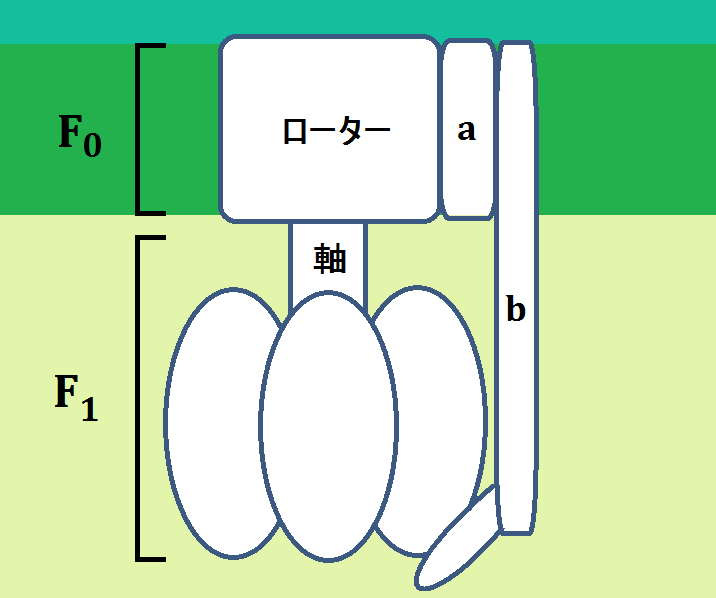
説明の為に、ポイントとなる部分だけデフォルメして描きましたが、厳密にはもっと入り組んでいて形も歪んでいます。
「ATP合成酵素」は、大きく「F0」と、「F1」に分けられています。
「a」の部分が「H+」をローターに導きます。
そして、「H+」が膜間腔から「F0」を通ってマトリックスへ移動すると、膜に埋まっている「ローター」と、その下の「軸」が回転します。
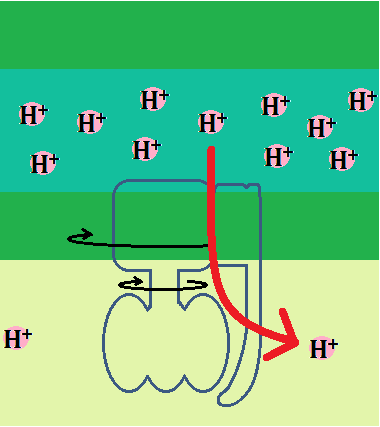
そして、マトリックス側にぶら下がって、「b」に固定されているのが「ATP」を合成するところです。
こちらが断面図です。正確に言うと、中心の軸は非対称になっています。
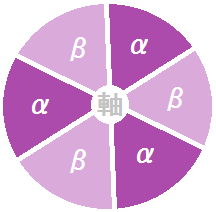
「α」と「β」の2種類のサブユニットが、3個ずつ交互に並んでいます。
この部分が立体構造を変えながら、「ADP」と「リン酸」から「ATP」を作ります。
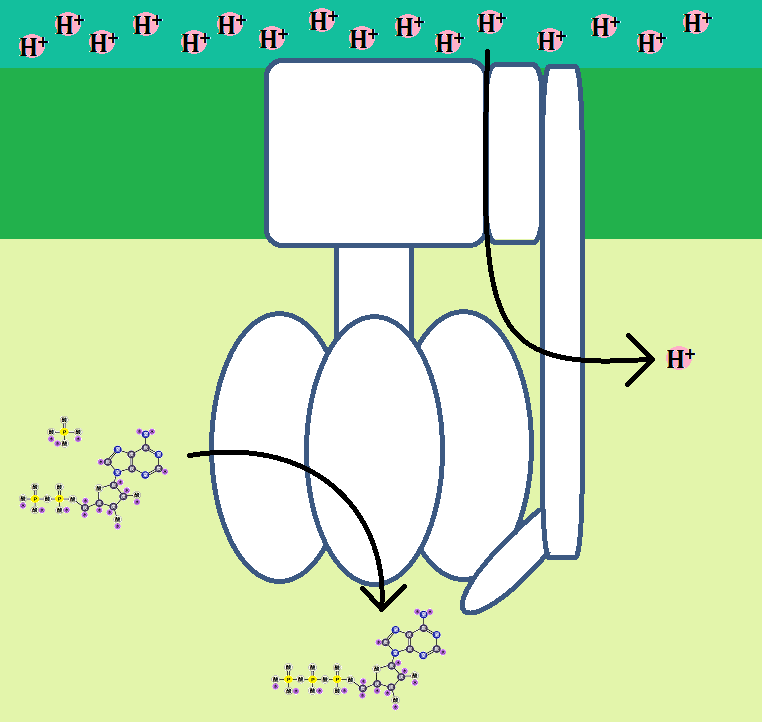
一方、マトリックスに戻った「水素イオン(H+)」は、再び膜間腔に放出されたり、水分子の生成の為に取り込まれたりします。
最後に
始めにお話した通り、「電子伝達系」については、私も迷いながら書いています。
説明の内容だけでなく、複合体の形まで人によって言うことが違うからです。
それに、複合体の説明ででてくる専門用語を調べている過程で、「まだ解明していない」という記述も何度か読みました。
そもそも、目に見えない世界なので、情報が食い違っていても、何が間違いで、何が正しいのか確認しようがありません。
確証がない事を書くのは嫌いなのですが、今後健康の事を語っていく上で外せない部分です。なので、迷っているところや、分からないところを含めてそのまま記事にしました。
間違っているところもあると思いますが、さすがに全て間違いということはないので、鵜呑みにせず、参考程度にとどめていただければと思います。
なお、記事全体としても気に入らないところが多いので、本記事は時々修正します。
スポンサーリンク