- 投稿
- 分かりやすいシリーズ
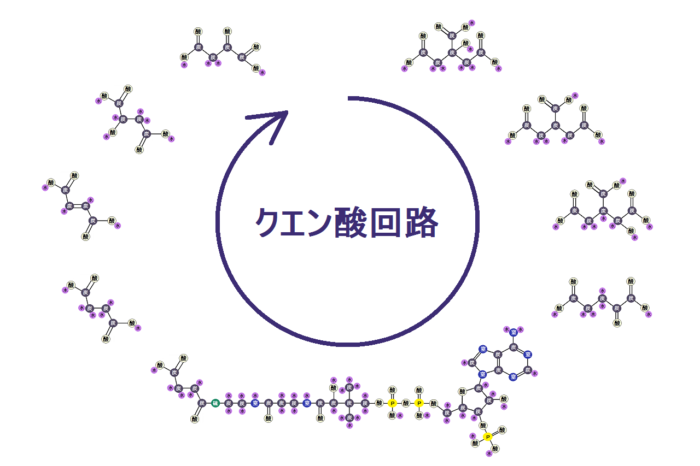
本記事では、「クエン酸回路」の流れを、「解糖系」でできた「ピルビン酸」から説明していきます。
以下の記事をまだお読みでない方は、先にこちらから読むことをオススメします。
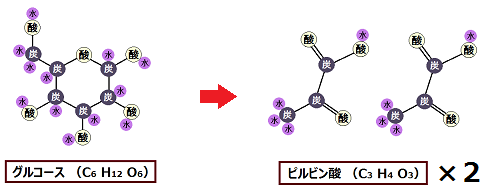
「解糖系」によって、1分子の「グルコース」から、2分子の「ピルビン酸」が生じました。
「クエン酸回路」は、ミトコンドリアのマトリックスで起きるので、ピルビン酸は「細胞質基質」から「マトリックス」に移動します。
ミトコンドリアは、2重の膜で覆われていて、膜は「リン脂質」という油成分でできています。
そして、「外膜」には、膜を貫通している「ポーリン」と呼ばれる、タンパク質でできた「低分子物質の通路」があります。この通路は分子量5000以下の親水性の分子を通すので、ピルビン酸のような小さな物質は自由に通過できます。
しかし、「内膜」には「ポーリン」はありません。
なので、ピルビン酸は、膜に埋め込まれている「ピルビン酸トランスロカーゼ」というタンパク質によって、マトリックスに運ばれます。
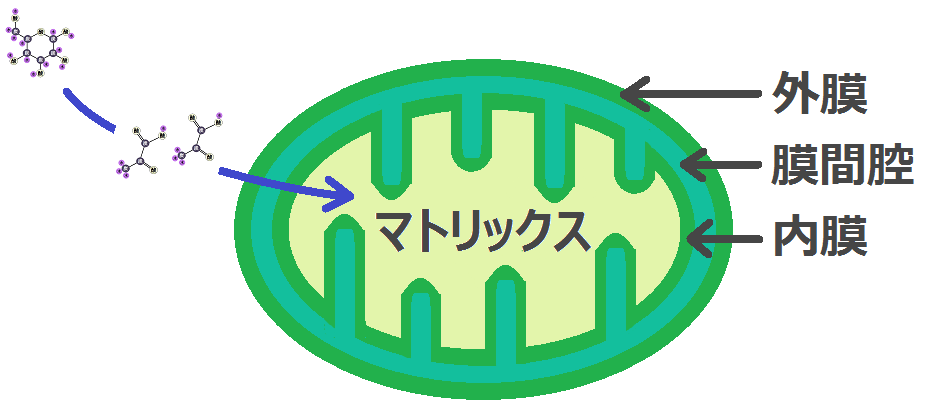
マトリックスで「クエン酸回路」の反応が起きるのですが、
その為にはまず、「ピルビン酸」が「アセチルCoA」に変換される必要があります。
スポンサーリンク
【序章】ピルビン酸 → アセチルCoA
「CoA こえー」って何だ?・・・という人の為に、先に「CoA」について解説しておきます。
「CoA」の正式名称は、「コエンザイム A / 和名:補酵素A」です。
「補酵素 ほこうそ」というのは、「酵素ではないけど、酵素の反応に協力しているサポート役」です。そして、「CoA」の「A」は、最初に発見されたという意味です。
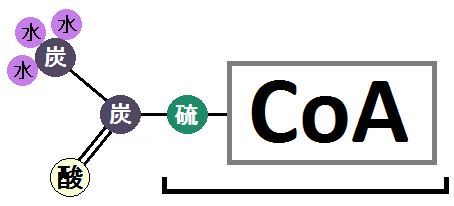
以下が「CoA」の構造になります。
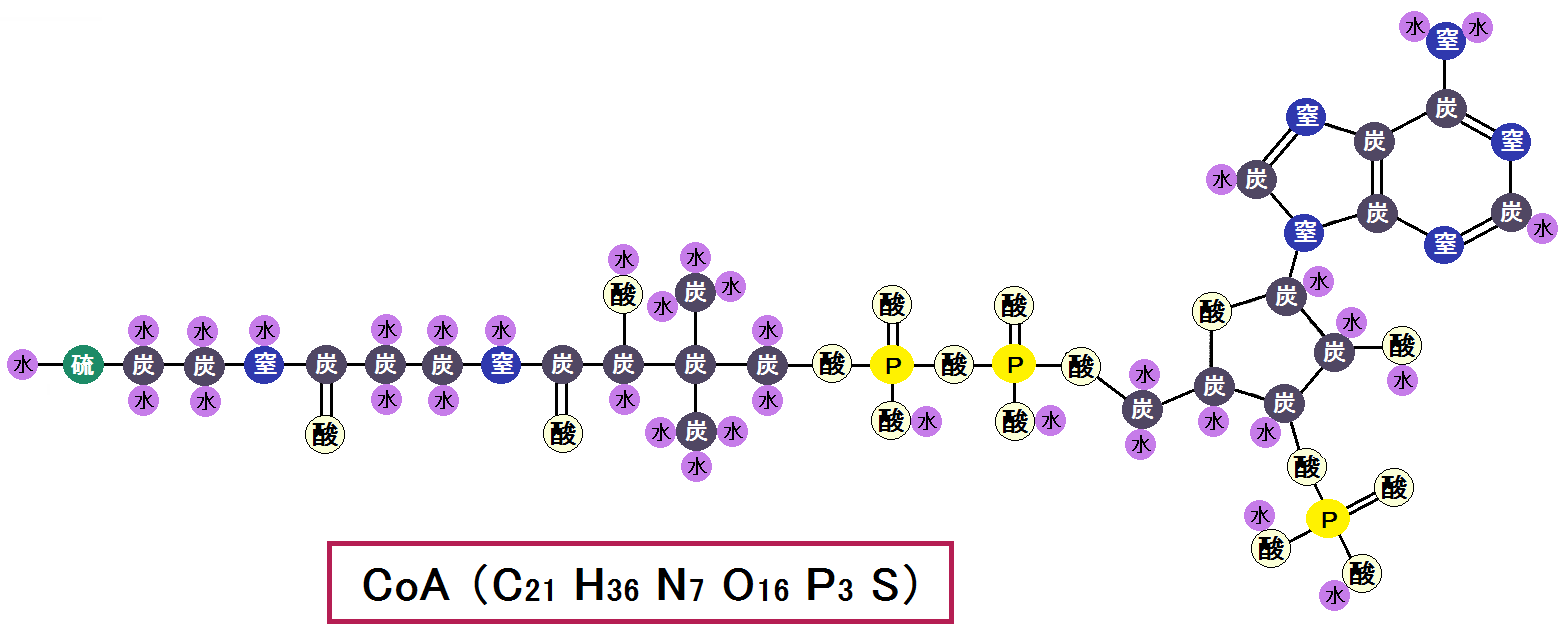
本記事で使用する絵ですが、通常は、炭素(C)、酸素(O)、水素(H)、窒素(N)、硫黄(S)、リン(P)と書くのですが、英語よりも日本語の方が親しみやすいので漢字にしました。
ただし、リン(カタカナだと見栄えがイマイチ)は英語にしました。
「CoA」は高エネルギーで、様々な基質と結合します。これがくっつくと活性化されるので、その後の反応が進みやすくなります。
「〇〇〇 CoA」・・・という物質は多く、クエン酸回路でも「アセチルCoA」の他に「スクニシルCoA」が登場します。「CoAがついた化合物」は、不安定でエネルギーを放出しやすい状態です。
それでは話を戻します。
「クエン酸回路」を進めるには、まず「ピルビン酸」を「アセチルCoA」に変えなければなりません。
この反応の酵素は、「ピルビン酸デヒドロゲナーゼ複合体(脱水素酵素)」です。
名前は「脱水素(水素が外れる)」ですが、「脱炭酸(二酸化炭素が外れる)」と「CoAによる活性化」の反応も起こす、巨大で複雑な酵素です。だから「複合体」なのです。
そして、以下が反応が起きる前のそれぞれの状態です。NADの説明は解糖系の記事でお話しました。
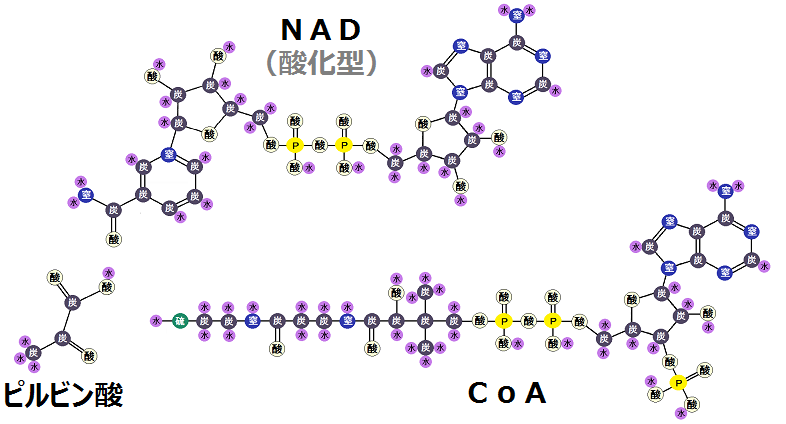
反応後、「ピルビン酸」、「CoA」、「酸化型NAD」は、こうなります。
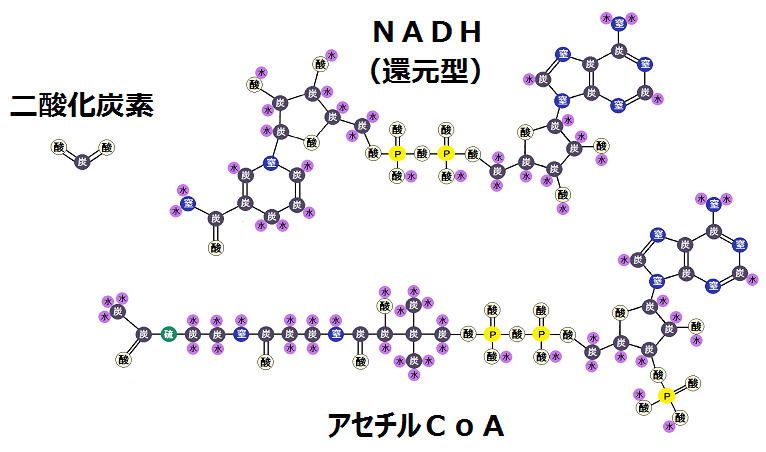
それぞれがどのように変化したのか、順に説明します。
「ピルビン酸」からは、炭素が1個と、酸素が2個外れます。つまり、二酸化炭素(CO2)です。普段私たちが吐いている息はここで生じるわけです。
二酸化炭素(CO2)が取れることを「脱炭酸反応」と言います。
しかし、今回のように酸化(水素を失う)と同時に脱炭酸する場合は「酸化的脱炭酸反応」と言います。
そして、残った「ピルビン酸」はこうなりました。
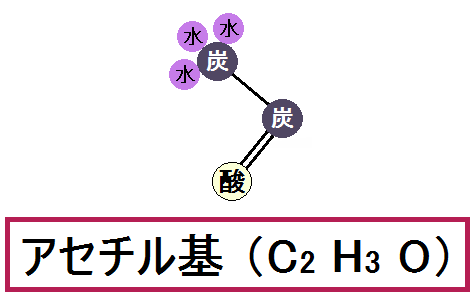
これを「アセチル基」と言います。
これが、先ほど説明した運搬役の「CoA」とくっついて、「アセチルCoA」になります。
「CoA」の一番左にあった「水素」が外れて、硫黄の横に「アセチル基」がくっつきます。
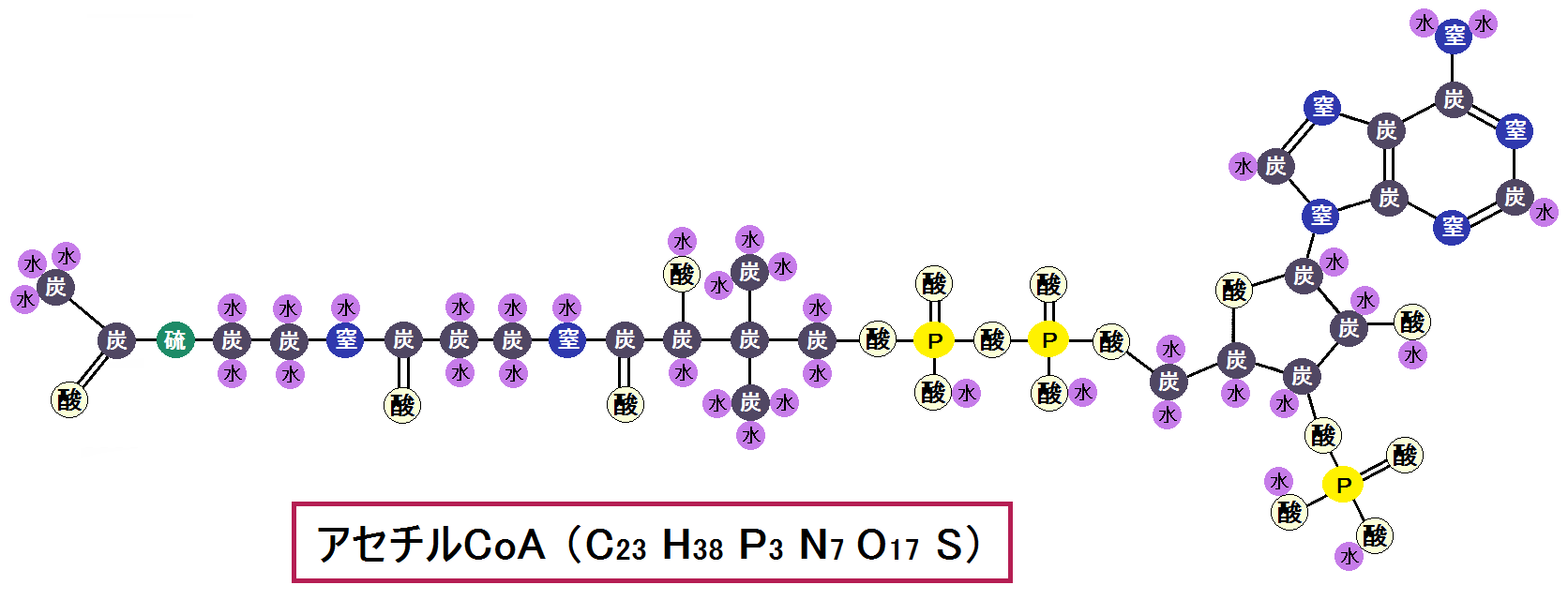
ちなみに、この「アセチルCoA」が省略される時、何故かこのように硫黄(S)を外に出して書きます。
そして、酸化型だった「NAD」は、水素を受け取って還元型の「NADH」になります。
「アセチル基」は、炭素は「クエン酸回路」で二酸化炭素になり、水素はNADやFADに預けた後、「電子伝達系」を経て水分子になるので、化学的に分解されます。
それでは、「アセチルCoA」になったので、ここからは「クエン酸回路」のスタートです。
①アセチルCoA → クエン酸
ここまでの流れを俯瞰でみます。「クエン酸回路」はこのような順番で進みます。
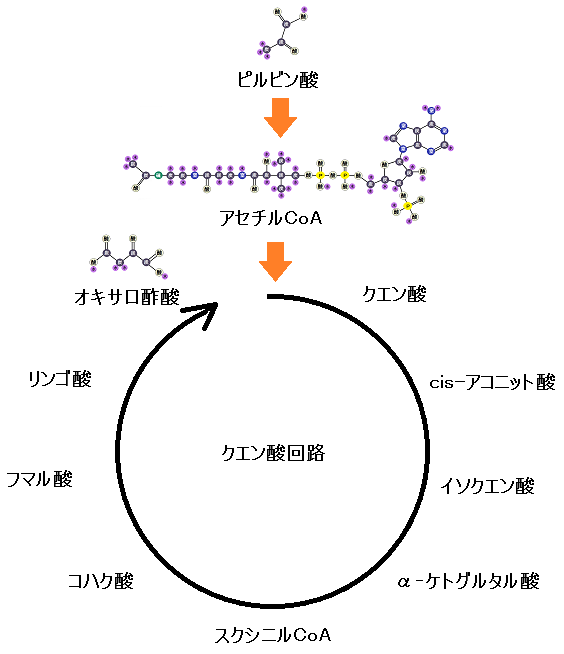
「クエン酸」から始まるから「クエン酸回路」です。回路という名前の通り、一周して終わりではなく、何度もくるくると回ります。
まず、「アセチルCoA」は、「オキサロ酢酸」と出会います。ここで出合った「オキサロ酢酸」は、前のクエン酸回路の反応でできた化合物です。
以下が、「アセチルCoA」と、「オキサロ酢酸」、そして「水分子」です。
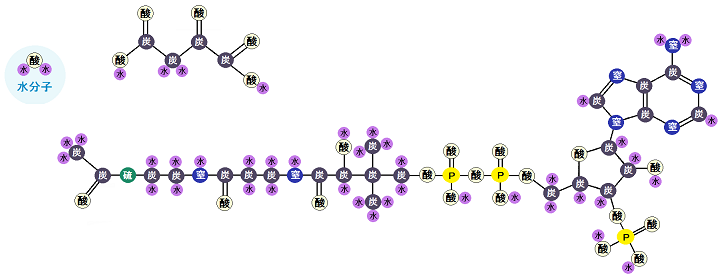
「クエン酸シンターゼ」という酵素が、これらを基質にして、「クエン酸」と「CoA」を合成します。
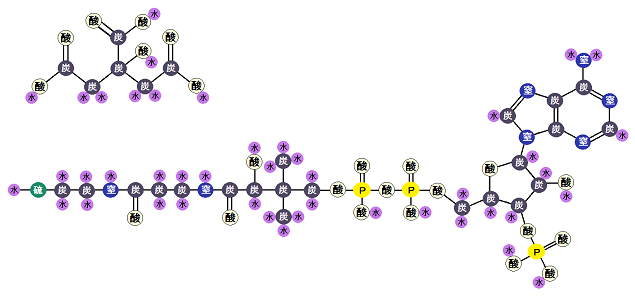
「アセチルCoA」は、「アセチル基」が外れたことで「CoA」に戻ります。
「CoA」は、基質と結合してここまで運んできましたが、あくまでサポート役で、「クエン酸回路」に組み込まれるわけではないので退場します。
「クエン酸」だけが次の反応へ進みます。
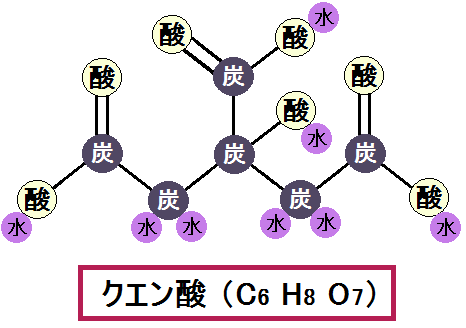
②クエン酸 → (Cis-アコニット酸) → イソクエン酸
「クエン酸」から1つの酵素で、2段階の反応が起きます。なので、中間の「Cis-アコニット酸」は省略されることがあります。
酵素の名前は、「アコニット酸ヒドラターゼ(アコニターゼ)」です。
まず、「クエン酸」から「水分子」が出て「Cis-アコニット酸」になります。
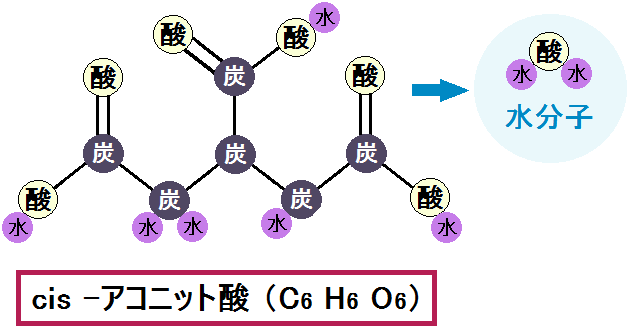
そして、その水分子が加わって、配置が変わる事で「イソクエン酸」になります。
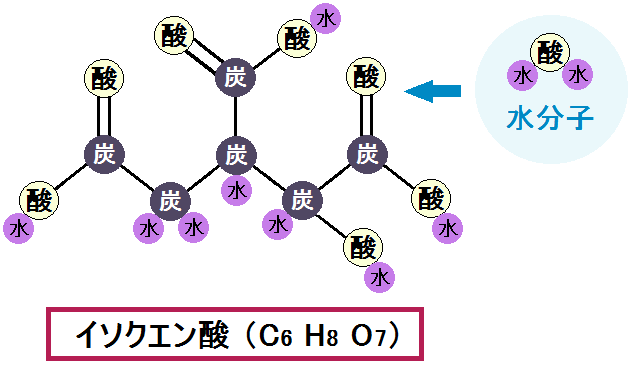
イソクエン酸は次の反応に進みます。
③イソクエン酸 → (オキサロコハク酸) → α-ケトグルタル酸
この反応も「イソクエン酸脱水素酵素(デヒドロゲナーゼ)」という1つの酵素によって、2段階の反応が起きます。なので中間の「オキサロコハク酸」は省略されることがあります。
この反応では「脱水素」と「脱炭酸」が起きます。
反応前の状態がこちらです。
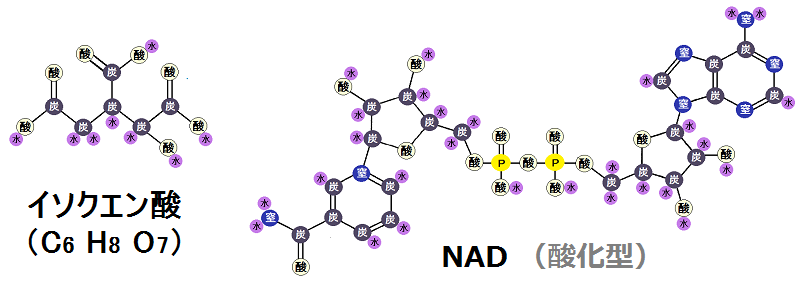
酸化型の「NAD」は、「イソクエン酸」の水素を奪って、還元型の「NADH」になります。
すると、不安定な「オキサロコハク酸」になります。
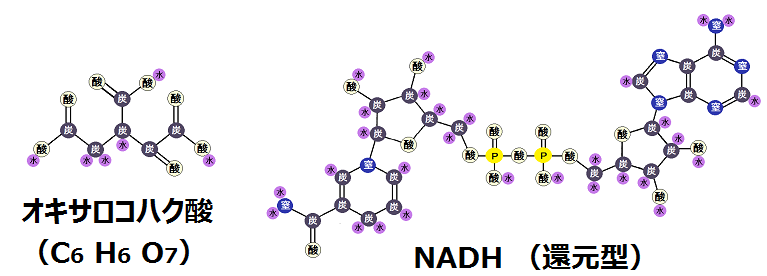
「オキサロコハク酸」は脱炭酸され、「α-ケトグルタル酸」と「二酸化炭素」が生じます。
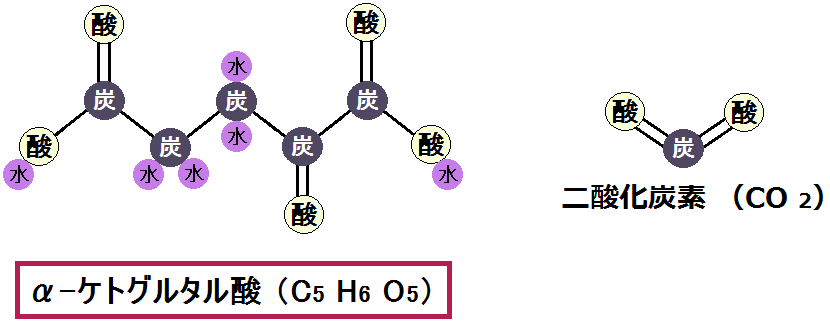
「αーグルタル酸」は、「2-オキソグルタル酸」とも言います。
というわけで、「α-ケトグルタル酸」は次の反応に進みます。
④α-ケトグルタル酸 → スクニシルCoA
ここでは「ピルビン酸 → アセチルCoA」になった時と似たようなことが起きます。
以下が反応前の状態です。
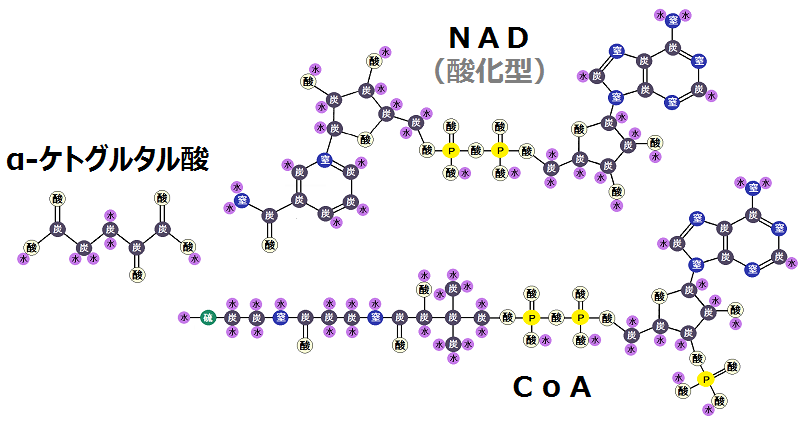
酵素「α-ケトグルタル酸(2-オキソグルタル酸)デヒドロゲナーゼ複合体」によって、「脱水素」と「脱炭酸」が起きます。
そして、高エネルギーな補酵素「CoA」がついて、「スクニシルCoA」となります。
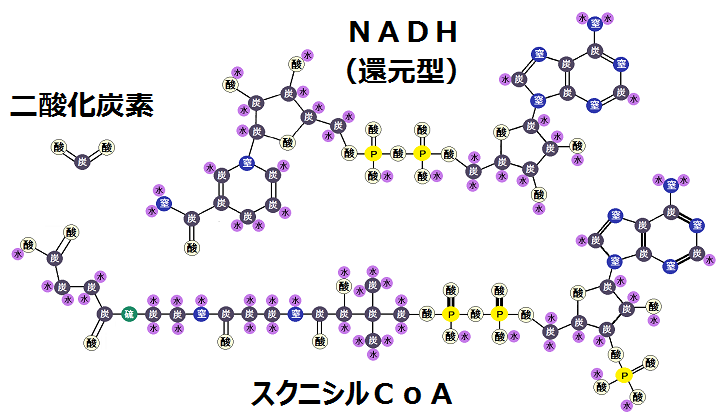
構造はこうなっています。
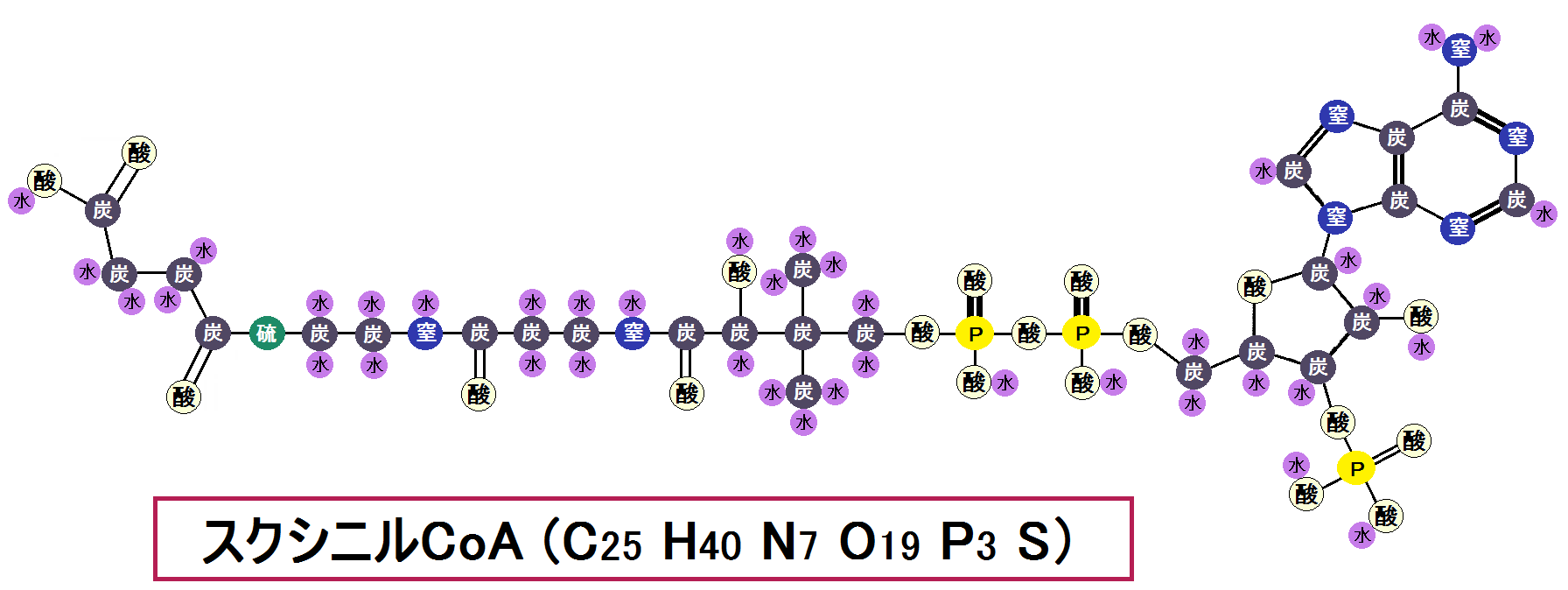
これも長いので、以下のように省略されます。
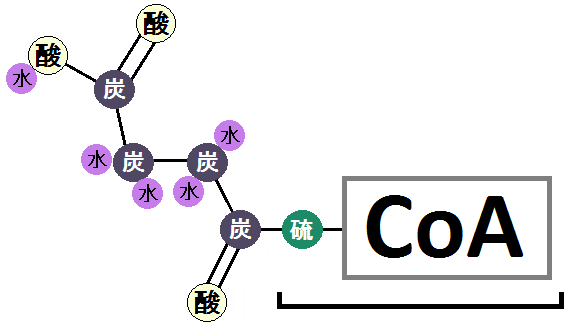
スクニシルCoAは次の反応に進みます。
スポンサーリンク
⑤スクニシルCoA → コハク酸
ここで、また新しい物質が出るので、反応の説明の前に先に紹介します。
名前は「GTP ジーティーピー」と言って、このような構造になっています。
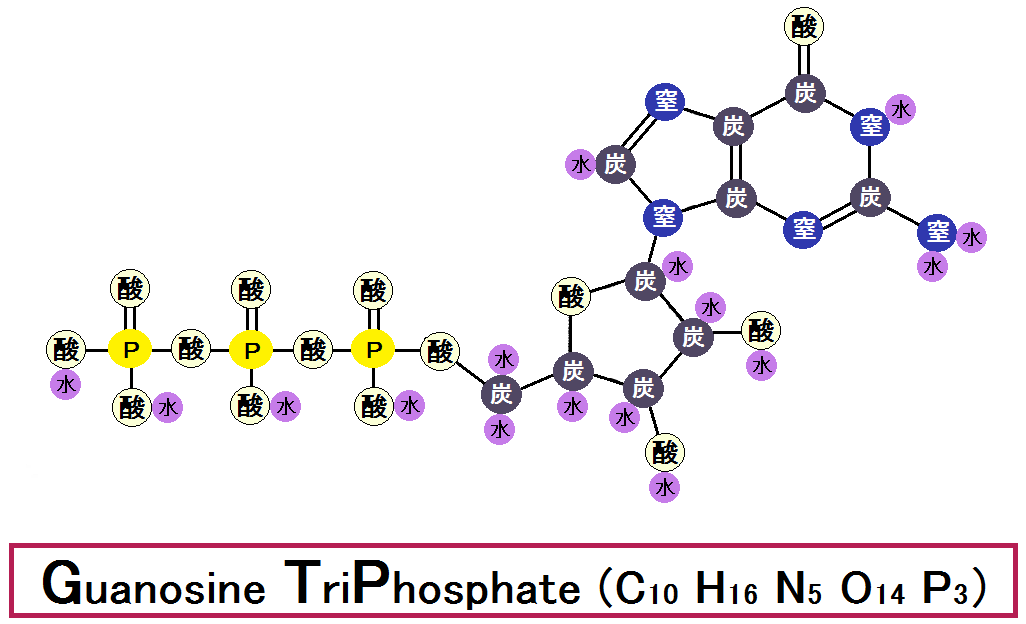
「グアノシン・トリ・ホスフェート / 和名:グアノシン3リン酸」と言い、リン酸基が3つ付いています。
名前も構造も「ATP」によく似ています。
「ATP」は、リン酸が3つくっついていて、リン酸が1つ外れる時にエネルギーが放出され、「ADP」になりますが、「GTP」も3つあるリン酸のうち1つが外れる時にエネルギーが放出されます。
こちらがエネルギーが放出された後の「GDP ジーディーピー」です。
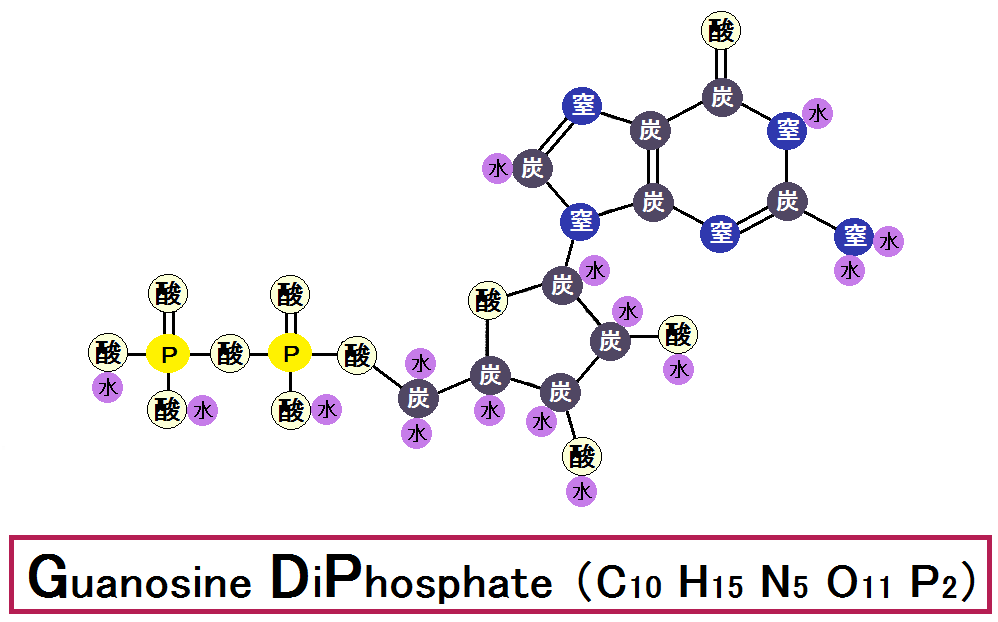
「グアノシン・ジ・ホスフェート / 和名:グアノシン2リン酸」と言い、リン酸基は2つです。
それでは話を戻します。
以下が反応前の状態です。
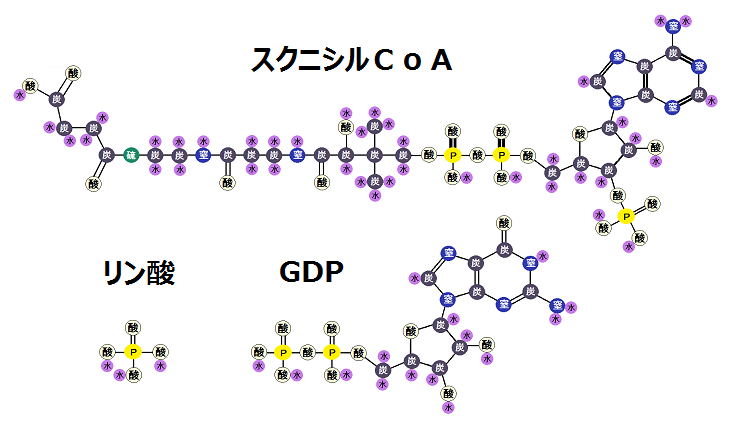
この反応で使われる酵素は「スクニシルCoAシンターゼ」です。
これによって、「スクニシルCoA」から「CoA」を外す時のエネルギーで、「GDP」と「リン酸」から「GTP」が合成されます。
出来上がった「GTP」は、高エネルギーの化合物です。
そして、「GTP」はリン酸が3つあるわけですが、このうちの1つを「ADP」に与えます。この時使われる酵素は「ヌクレオシド2リン酸キナーゼ」です。
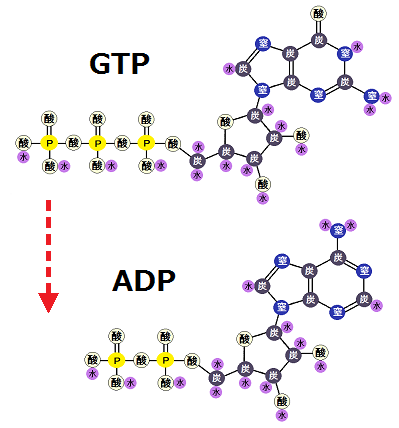
リン酸をあげたことで「GTP」は「GDP」になり、「ADP」は、リン酸3つの「ATP」になります。つまり、「ATP」が合成されたということです。
そして、「スクニシルCoA」は「コハク酸」になります。
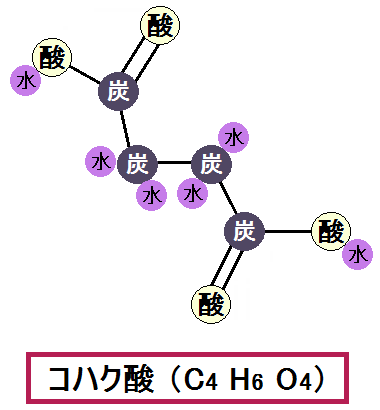
「コハク酸」は次の反応に進みます。
⑥コハク酸 → フマル酸
ここで、また違う物質がでてきます。
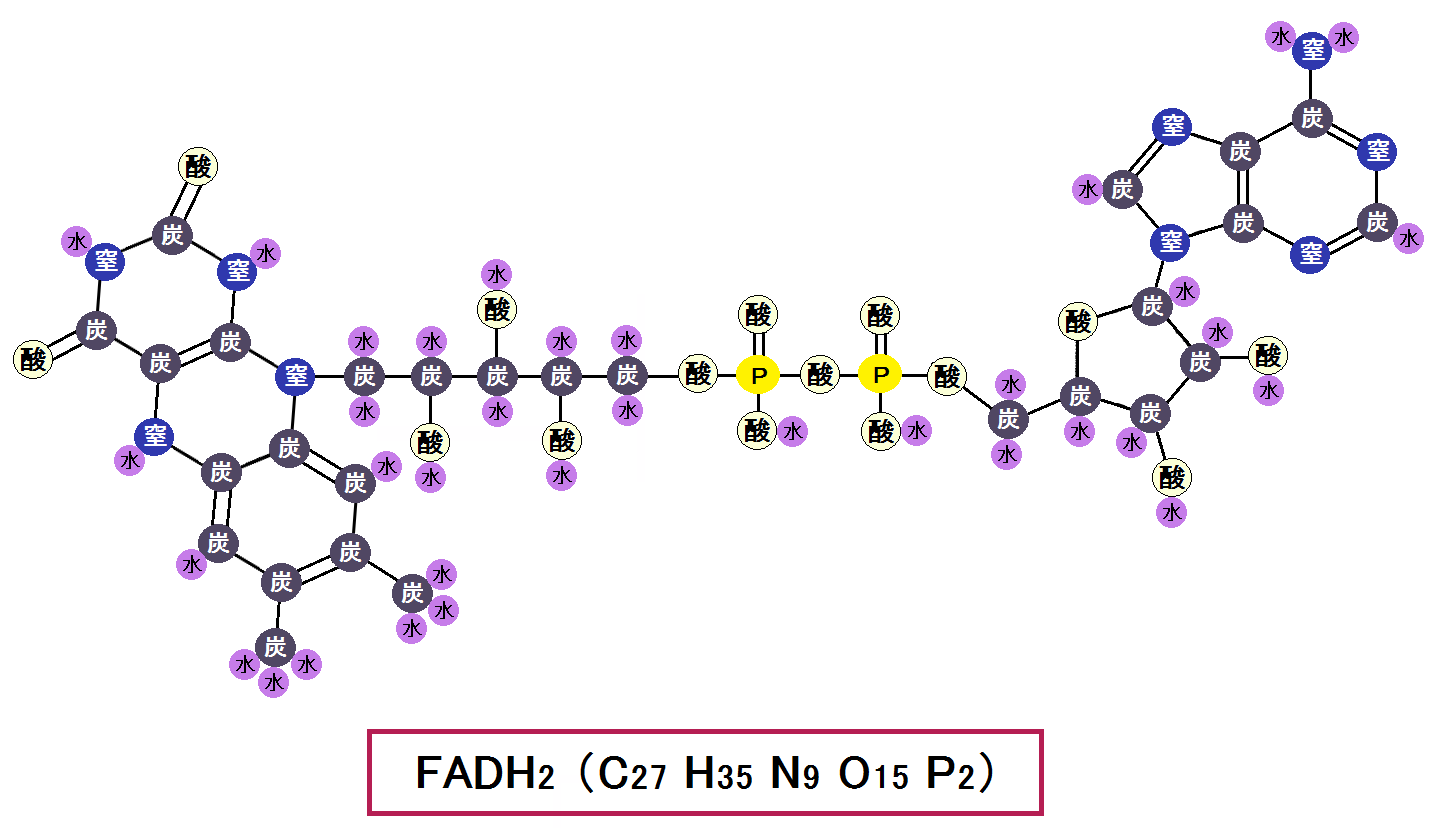
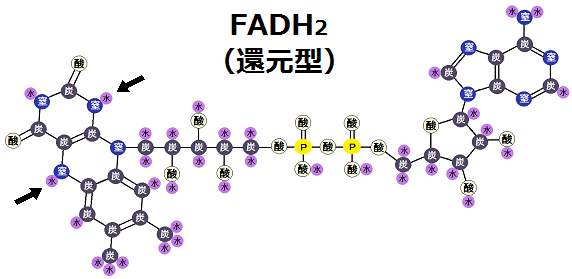
「FAD エフエーディー」という補酵素です。構造は以下になります。
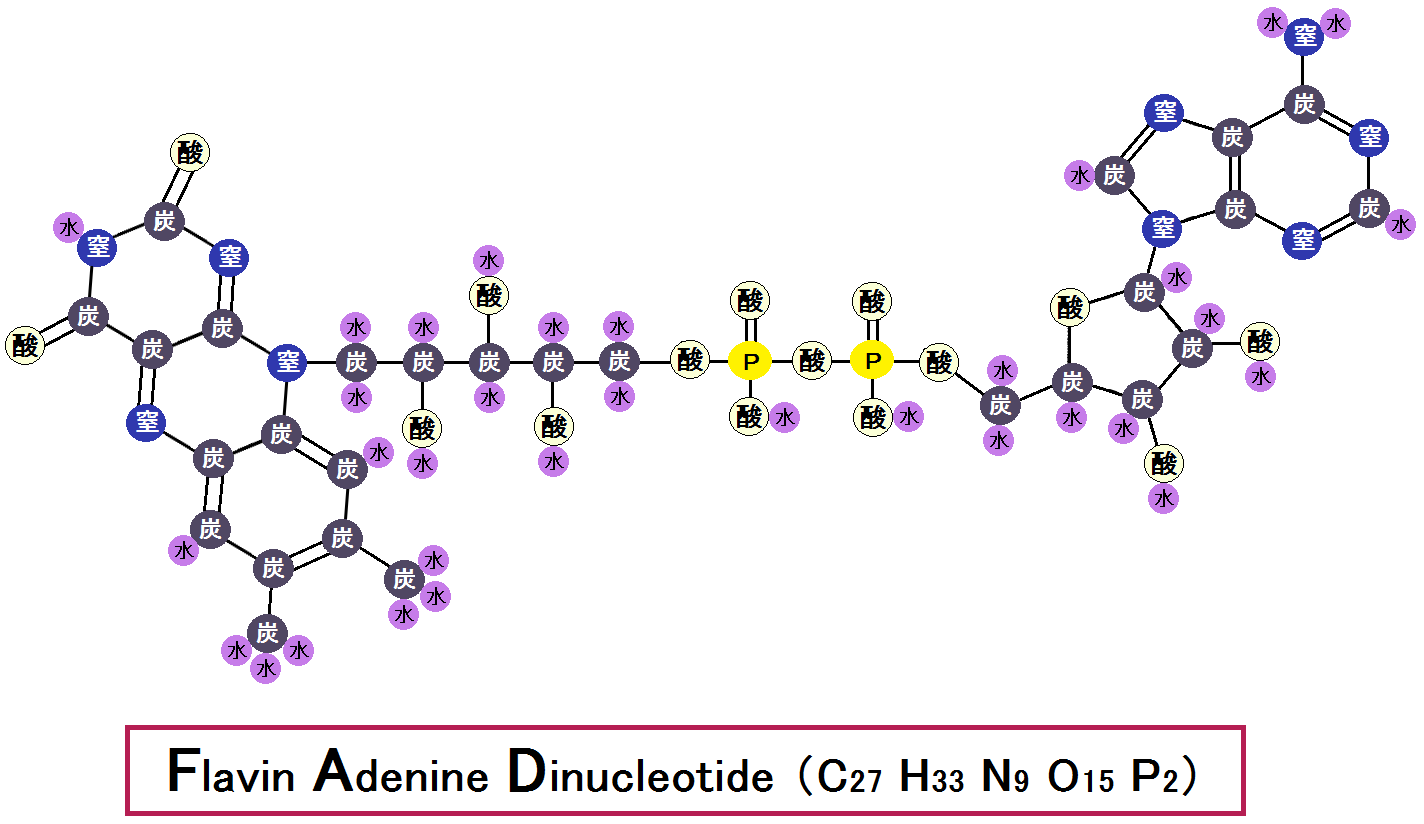
「フラビン・アデニン・ジヌクレオチド」と言い、「NAD」と同じで、水素(の持つ電子)の預かり役「電子伝達体」です。
酸化型の「NAD」は、水素を預かることで、還元型の「NADH」になりましたが、「FAD」も酸化型が水素を預かると、還元型の「FADH2」になります。
では、話を反応に戻します。
以下が反応前の「コハク酸」と酸化型の「FAD」です。
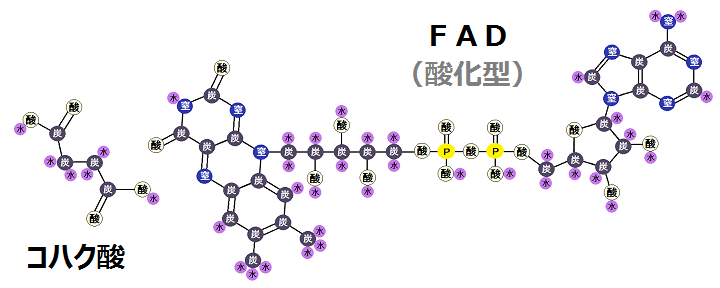
脱水素(酸化還元)酵素である「コハク酸デヒドロゲナーゼ複合体」によって、「コハク酸」は「FAD」に水素を渡します。
すると、「FAD」は還元型の「FADH2」になり、「コハク酸」は「フマル酸」になります。
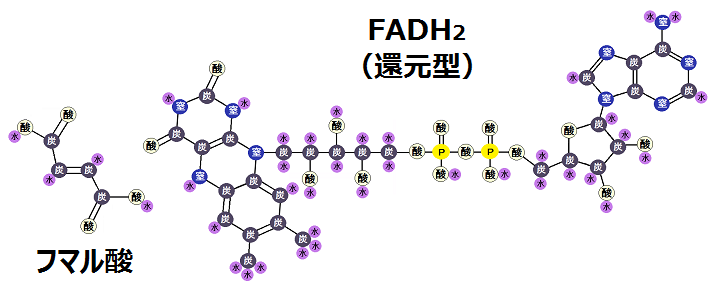
こちらが構造になります。
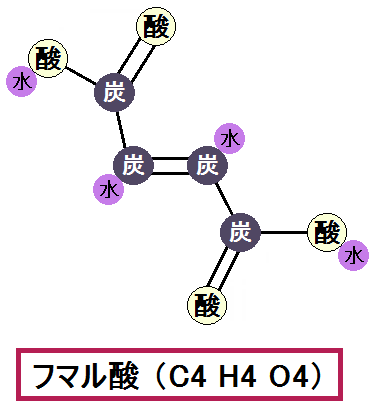
「フマル酸」は次の反応に進みます。
なお、この反応で使われた酵素「コハク酸デヒドロゲナーゼ複合体」は、電子伝達系の「複合体Ⅱ(コハク酸デヒドロゲナーゼ複合体)」と同じものです。
⑦フマル酸 → リンゴ酸
この反応では、「フマル酸ヒドラターゼ(フマラーゼ)」という酵素が使われます。
「フマル酸」に水分子(H2O)が加わります。
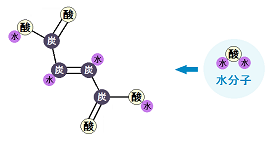
すると、「リンゴ酸」になります。
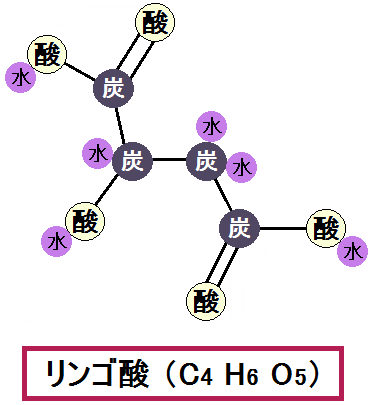
「リンゴ酸」は次の反応に進みます。
⑧リンゴ酸 → オキサロ酢酸
「クエン酸回路」最後の反応です。
この反応で使われる酵素は「リンゴ酸デヒドロゲナーゼ(脱水素酵素)」です。
以下が反応前の状態です。
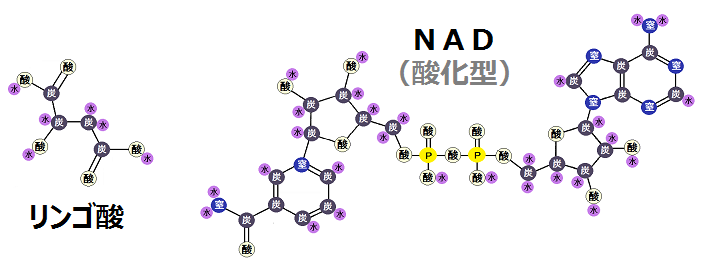
「リンゴ酸」が酸化型の「NAD」に水素を預けると、「NAD」は「NADH」に、そして、「リンゴ酸」は「オキサロ酢酸」になりました。
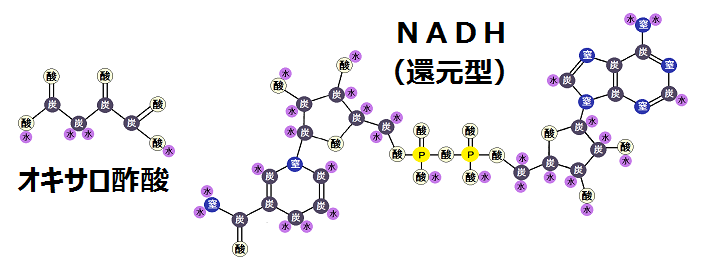
以下が、「オキサロ酢酸」です。
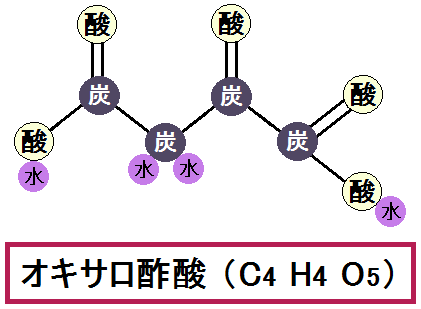
これで「クエン酸回路」を一周したことになります。
こうしてできた「オキサロ酢酸」が、また次の「アセチルCoA」と反応するわけです。
ピルビン酸デヒドロゲナーゼ複合体について補足
「ピルビン酸デヒドロゲナーゼ複合体」は、「複合体」とついているように、3つの酵素(E1、E2、E3)が集まった複雑な構造をしています。以下が1~3の酵素の名前です。
- E1・・・ピルビン酸デヒドロゲナーゼ
- E2・・・ジヒドロリポイルトランスアセチラーゼ
- E3・・・ジヒドロリポイルデヒドロゲナーゼ
そして、複数の補酵素が必要です。
アセチル基を受け取る「CoA」、水素原子を受け取る「NAD」の他にも、「FAD」、「チアミン2リン酸」、「α-リポ酸」が、酵素のサポートをします。
栄養の話になるのですが、
「CoA」の合成には、「ビタミンB5(パントテン酸」が、
「NAD」の合成には、「ビタミンB3(ナイアシン)」が、
「FAD」の合成には、「ビタミンB2(リボフラビン)」が、
「チアミン2リン酸(チアミンピロリン酸)」の合成には、「ビタミンB1(チアミン)」が、
それぞれ必要になってきます。
E1の「ピルビン酸デヒドロゲナーゼ」の補酵素「チアミン2リン酸」は、「ビタミンB1」の活性型です。
「ピルビン酸」→「アセチルCoA」に変える為に必要な補酵素は1つではありませんが、「ビタミンB1」が強調されるのは、複合体の中の最初の反応に必要だからでしょう。
でも、他の補酵素も必要です。
従って、この代謝を止めないためにも、ビタミンB群のサプリを飲むといいわけです。
例えばこれ。
B群が足りなくなるとどんな不具合が起きるのか、沢山のB群が必要な体質については以下の記事に書きました。
ベジタリアンや糖質を止められない人が、健康の為に摂っておきたい栄養素とは
そして、「α-リポ酸」は、ビタミン様物質(ビタミンに似た有機化合物)です。
話がそれましたが、「ピルビン酸」を「アセチルCoA」に変えるには、厳密には3つの酵素と、5つの補酵素が必要ということになります。
具体的にどういう流れでそうなるのか調べたのですが、人によって説明が食い違っていたり、それ以前に、私でも理解できる文章で書かれたものが見つからなかったので、分かり次第書き加えたいと思います。
また、「④α-ケトグルタル酸 → スクニシルCoA」で働く酵素、「α-ケトグルタル酸(2-オキソグルタル酸)デヒドロゲナーゼ複合体」も、3つの酵素から構成される複合体で、やはり5つの補酵素が必要になります。
スポンサーリンク
NADとFADについて
電子伝達体の「NAD」と「FAD」についての補足になります。
ここまでは省略していたのですが、酸化型の「NAD」は、正確には「NAD」の右上に「+」と書きます。このプラスは、「プラスの電荷を帯びている」という意味です。
「NAD」の相手、「イソクエン酸」を例に説明します。
「イソクエン酸」は、水素が8ですが、このうちの2つが外れます。
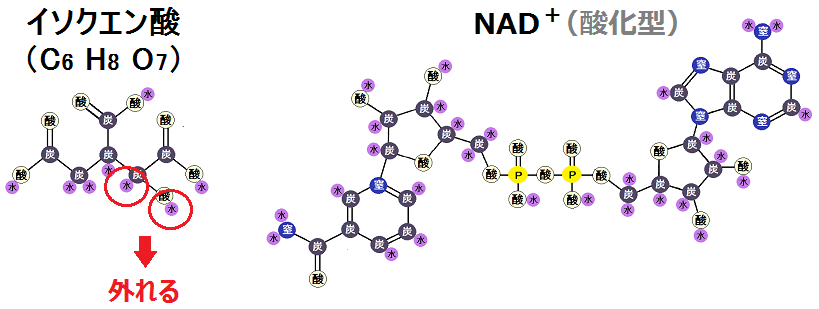
この外れた「水素原子」の構造はこのようになっています。
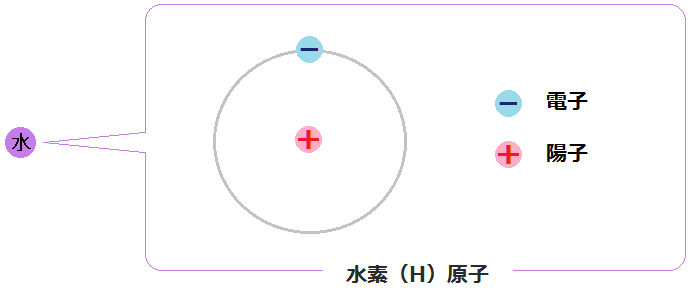
プラスの電気を帯びた「陽子(プロトン)」の周囲を、マイナスの電気を帯びた「電子(エレクトロン)」が衛星のように回っています。
「陽子」が1個と「電子」が1個のペア・・・これが「水素原子」です。
従って、「基質から水素が2個外れる」ということは、
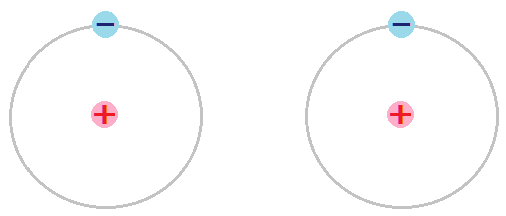
プラスの「陽子」が2つ、マイナスの「電子」が2つ外れるということになります。
で、「NAD+」の方は、プラスの電気を帯びています。「窒素+」のところです。
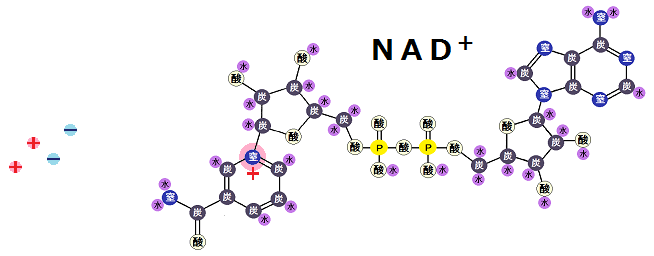
「NAD+」は、「電子(-)」2つと、「陽子(+)」1つを受け取ります。水素原子がくっついて、「窒素+」が「電子(-)」によって還元されます。
還元型に変わると、電気的に中性になります。
ですが、1つ「陽子(+)」が余ります。
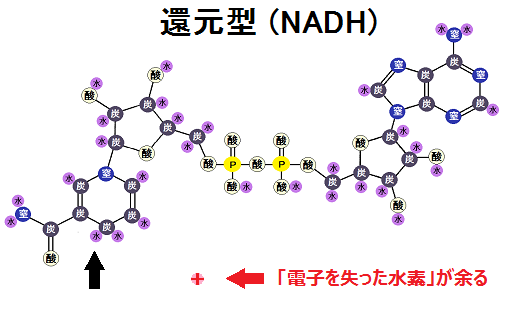
この「電子を失った水素」の事を「H+」、「水素イオン」、「プロトン」等と言います。
従って、「還元型のNADH」は、厳密には「NADH + H+」のセットということになります(※「H+」は遊離します)。
調べていると、情報源によって、酸化型は「NAD」と書かれていたり、「NAD+」と書かれていたり、また還元型は、「NADH」と書かれていたり、「NADH2」と書かれていたり、統一感がありません。「+」の意味、「2」の意味も、説明が回りくどくて何が言いたいのか分かりにくいものがほとんどで、納得するのに時間がかかりました。一番分かりやすかったのは以下の本です。
『イラスト 基礎からわかる生化学―構造・酵素・代謝 / 著者:坂本 順司』より引用
ナイアシンは分子中でアミドの形で存在しており、このニコチンアミド環がまさに酸化還元のおこる場所である。
酸化型では正電気を帯びており、電子(e-)2つと水素イオン(H+)1つを受け取って還元型に変わると、電気的に中性となる。
(中略)
酸化還元反応でNADやNADPの相手となる有機酸などの基質は、多くの場合2つの水素原子、いいかえると2つの e- と2つの H+ を解離・結合する。したがって両者が反応すると H+ が1つ遊離(逆反応の場合は吸収)される
(167p~168p)
そして、「FAD」について説明します。
酸化型の「NAD+」は、「電子(-)」2つと、「陽子(+)」1つを受け取るのですが、
酸化型の「FAD」は、「電子(-)」2つと、「陽子(+)」2つを受け取ります。なので、「NAD」のように陽子は余りません。
「コハク酸」で説明します。
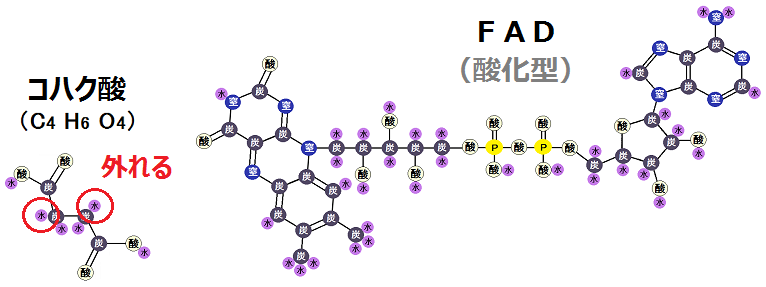
コハク酸の「水素原子」が2つ外れるので、「電子」2つ、「陽子」2つが外れるということになります。
一方、酸化型の「FAD」は、「電子」2つと、「陽子」2つを受け取るので、「水素原子が2つ結合した」ことになります。
従って、「FADH2」となります。
フラビンもナイアシン誘導体と同様、2電子酸化還元をおこなう補酵素である。ただしNADやNADPとは違い、2つの e- と同時に H+ も2つ授受するので、H+ が遊離・吸収されることはない
(169p~170P)
クエン酸回路のおさらい
クエン酸回路によって生じたものをまとめます。
【序章】ピルビン酸 → アセチルCoA
二酸化炭素(CO2)
①アセチルCoA → クエン酸
②クエン酸 → (Cis-アコニット酸) → イソクエン酸
③イソクエン酸 → (オキサロコハク酸) → α-ケトグルタル酸
NADH
二酸化炭素(CO2)
④α-ケトグルタル酸 → スクニシルCoA
NADH
二酸化炭素(CO2)
⑤スクニシルCoA → コハク酸
ATP
⑥コハク酸 → フマル酸
FADH2
⑦フマル酸 → リンゴ酸
⑧リンゴ酸 → オキサロ酢酸
NADH
そして、本記事に使用した絵は、以下の動画を参考にしました。分かりやすいアニメーションなのでオススメです。
こちらも合わせて見て下さい。
次は「電子伝達系」についてお話します。
電子伝達系(呼吸鎖)について分かりやすく説明してみた①複合体Ⅰ~Ⅱへ続く
スポンサーリンク


こんにちは。国立大医学科の1年生です。細胞生化学の勉強の参考としてありがたく使わせていただいております。
とてもわかりやすいです。ありがとうございます!
さて、口を出すようで誠に申し訳ないのですが、オキサロコハク酸のCO間やフマル酸のCC間などは二重結合ではないでしょうか?
また、次回以降グリコーゲン代謝や糖新生などについても解説いただけたら嬉しいです。
今後も、ブログの投稿よろしくお願いします。頑張ってください!
ゆうゆうさん、コメント有難うございます。
>さて、口を出すようで誠に申し訳ないのですが、オキサロコハク酸のCO間やフマル酸のCC間などは二重結合ではないでしょうか?
助かりました。ガッツリ間違えていました。わざわざ教えて下さり有難うございます。
「糖新生」は過去に記事にしました。よくできた動画を参考にした今回の記事程ではありませんが、よかったら読んでみて下さい。
糖新生の仕組みについて分かりやすく説明してみた
アリヤ様
返信ありがとうございます。
糖新生については記述されていたのですね!気づかずにすみません、、、。
またじっくり読ませていただきます。
はじめまして。大学受験を控えている高3です。
以前からアリヤ様の記事をどれも
興味深く読ませて頂いています。
私の体験についてアリヤ様にお話ししたいことがありますので、書かせてください。
私は中学生でダイエットを始めたのをきっかけに健康に興味を持つようになりました。
最初はただ痩せることが目的で、
米、揚げ物、肉、パン、お菓子やアイスを断ち減量に成功しました。
野菜、魚、豆腐や味噌汁、お吸物を中心とした食事に加え、私は牛乳とグラノーラが好きでこれだけはやめられなかったので、グラノーラの材料を自分で購入し手作りして朝食にしていました。
この頃は肌が血の気がないほど白く、爪も紫ではなく白に近くなり、冷えや低体温に悩んでいました。
高校生になって食事の制限を緩め、果物や肉を次第に口にするようになりました。
ある時、鏡を見て自分の顔が黄ばんでいることに気づき、調べたところ「糖化」についてのアリヤ様の記事にたどり着きました。
私はほぼ毎日朝食にりんご半分食べていたので、これが原因だとすぐにわかりました。(高校に入ってからグラノーラ作りはやめています)
それから米を食べるようになり、私の体調は悪化し始めました。とはいいますが、食べ始めたころはタンパク質と脂質が十分摂れていたので、中学生の頃の不調はなくなりました。この時に私はタンパク質を摂っていても脂質が不足していた危ない状態だったことにきづくことができました。
そして今年になって、受験のストレスやエネルギー不足を糖質で対処するようになりました。今まで糖質をほどんど摂取していなかったので、いつのまにか糖質依存に陥り、肉が美味しいと感じなくなりました。焼肉でも、以前は肉と野菜でいくらでも食べれるほど胃は強かったのに、最近は特に牛肉で胃がもたれます。翌日に熱が出る程体調は優れません。なのにお菓子や米は食べれるのです。肉は体質に合わないと決めつけるところでした。
今日、生物のクエン酸回路を詳しく調べようと検索したところ、アリヤさんの記事を読みました。体調面でも勉強面でも私の疑問は解決しました。本当にありがとうございます。
長くなりましたが、アリヤ様に私のような高校生でもアリヤ様の記事を読んでいると知らせたかったでのです。そしてこの体調の変化のことも。
アリヤ様の意見は根拠があり、深く勉強された知識でいつも納得することができています。
受験生としてこのままの体質ではいけないと思うので、プロテインを取り入れ、糖質制限を始めたいと思います。最近またココナッツオイルを使ったグラノーラをつくりはじめたので(グラノーラと牛乳をやめて甘い物の欲求が強くなりました)、これまでの体験を活かして健康な身体になります。また、更年期である母とサプリメントを始めてみようと思います。
どうも野菜に栄養が少ないのではと私も思うからです。
まとまりのない文章で申し訳ありません。
これからも記事の更新を楽しみにしています。
アレンさん、コメントありがとうございます。
中学生の時から栄養の管理をされているのは素晴らしいですね。
現在は体調不良があったとしても、努力をされているので、方向性を間違えなければ、かなり体質改善ができると思います。
>グラノーラをつくりはじめたので(グラノーラと牛乳をやめて甘い物の欲求が強くなりました)
これはグラノーラと牛乳を止めたことが原因というよりも、これらに含まれている栄養素が絶たれたため甘い物欲求が強まった可能性もあると見た方がいいかもしれません。
アレンさんは内容から察すると女性の方だと思うのですが、その場合は「フェリチン」を測るなどして、鉄不足になっていないか注意した方が良いです。
肉が苦手になると、動物性のヘム鉄を摂る機会も減ります。
藤川徳美医師 facebook 2018年9月16日
で、ストレスですが、栄養で対抗する方法もあります。
藤川徳美医師 facebook 2018年8月6日
これは「ATPセット」ですね。
サプリを始めるならこの基本からが効率がよいです。
グラノーラの食感は私も好きで糖質制限をする前はよく食べていました。
グラノーラはドライフルーツが混ぜられていますが、果物に含まれている果糖はブドウ糖の10倍糖化しやすいです。
乾燥して濃縮されているので、グラノーラに混ぜる場合は量に気をつけた方がいいかもしれません。
アレンさんは手作りをされる方なので、試しに、プロテインを使ったお菓子など作られてみてはいかがでしょうか?
糖化も防げますし、プロテインも摂取できて一石二鳥です。
以下の記事のコメント欄で筋肉破無星さんが作り方を紹介して下さっています。
腸内環境が悪化する原因と、糖質制限で便秘になる場合の対策
この記事ではないのですが、もじゃこさんもプロテインをゼラチンで固めてババロア風にしたり、生クリームを追加してアイスにしたりと作り方を教えて下さいました。
栄養状態を良くすることで、能力が最大限発揮できるようになります。
おそらく受験勉強も効率よくこなせるようになるのではないかと思います。